V.2. Compuși ionici.
V.2.1. Formarea compușilor ionici.
Compușii ionici se formează în două etape:
1. Transfer de electroni (ē) de la metale la nemetale cu formarea ionilor pozitivi și negativi.
2. Atracția electrostatică între ionii de semn opus, fiind legătura chimică (legătură ionică) care se stabilește între ionii de semn contrar. Se formează un compus ionic stabil și neutru din punct de vedere electric (nr sarcini pozitive = nr sarcini negative), întotdeauna între două elemente cu caracter diferit (metale cu nemetale).
Exemple:
a) Sarea de bucătărie: Clorura de sodiu: NaCl
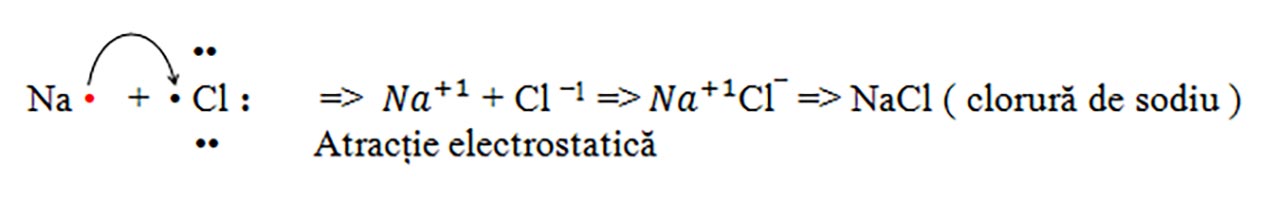
b) Clorura de magneziu: MgCl2
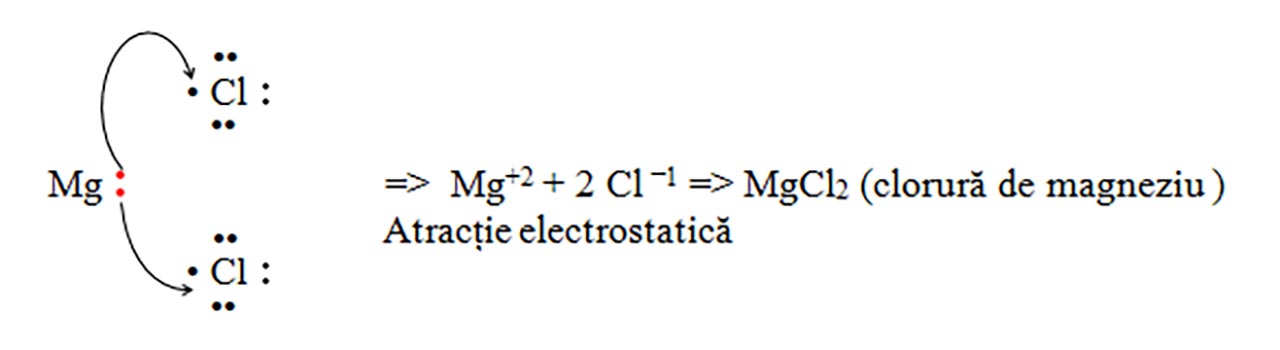
c) Clorura de aluminiu: AlCl3

👀 Experiment: Identificarea cationilor
🔥 Atenție! Acest experiment se efectuează numai de către profesori!
Materiale necesare:
Mină de grafit și soluții de NaCl, KCl, CaCl2, BaCl2, CuSO4
Descrierea experimentului:
- Se îmbibă mina de grafit în soluții de NaCl, KCl, CaCl2, BaCl2, CuSO4 și se ține în
flacăra unui bec Bunsen(aragaz).
Flacăra se colorează în diferite culori.
Concluzia experimentului:
Prezența unor cationi într-un compus ionic poate fi pusă în evidență prin colorarea diferită a flăcării de către
aceștia, astfel:
-
Na(+1) colorează flacăra în galben-închis
-
K(+1) colorează flacăra în violet
-
Ca(+2) colorează flacăra în roșu-deschis
-
Ba(+2) colorează flacăra în galben-verzui
-
Cu(+2) colorează flacăra în verde-închis
-
Cu(+1) colorează flacăra în albastru
-
Fe colorează flacăra în maroniu
-
Zn(+2) colorează flacăra în verde-albăstrui
-
Pb(+2) colorează flacăra în albastru
🔓 Problemă rezolvată
3. Modelează formarea compusului ionic dintre potasiu și sulf.

Rezolvare:
Pentru a obține un compus ionic, neutru din punct de vedere electric, trebuie să avem doi atomi de potasiu care să cedeze împreună doi electroni atomului de sulf.

V.2.2. Proprietățile fizice ale compușilor ionici.
👀 Experiment: Proprietățile fizice ale compușilor ionici
🔥 Atenție! Acest experiment se efectuează numai de către profesori!
Materiale necesare:
4 pahare Berzelius cu apă, baghetă, spatulă, circuit electric cu baterie, fire și bec, NaCl, CuSO4,
K2Cr2O7, BaCl2.
Descrierea experimentului (Partea 1):
- Analizați substanțele din cele 4 probe și stabiliți asemănările și deosebirile dintre proprietățile lor fizice
observabile.
Substanțele ionice sunt solide, divers colorate și cristaline (forme de poliedru). Cristale cubice de sare (NaCl) privite sub microscop.

-
Testează conductibilitatea electrică a substanțelor ionice, atât în stare solidă, cât și dizolvate în apă sub formă de soluții.
În stare solidă, compușii ionici nu conduc curentul electric.
În soluție și în topitură, compușii ionici conduc curentul electric. -
Verifică solubilitatea în apă a celor 4 probe.
Marea majoritate a compușilor ionici sunt solubili în apă.
Proprietățile fizice ale compușilor ionici:
-
Substanțele ionice sunt solide, divers colorate și cristaline.
-
Marea majoritate a compușilor ionici sunt solubili în apă.
-
În stare solidă compușii ionici nu conduc curentul electric.
-
În soluție și în topitură compușii ionici conduc curentul electric.