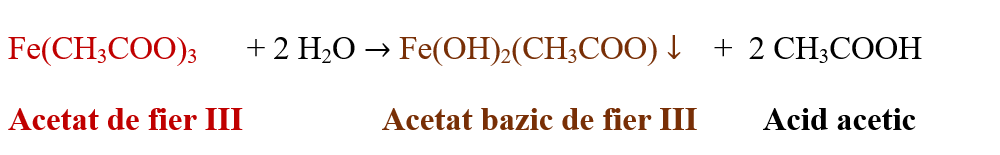VI.2.3.2. Identificarea cationului de fier
👀 Experiment: Identificarea cationului de fier II (Fe2+) cu hidroxid de sodiu
🔥 Atenție! Hidroxidul de sodiu este caustic!
🔥 Atenție! Sulfatul de fier II este coroziv și periculos pentru mediu !
Materiale necesare:
Sticlă de ceas sau eprubetă, soluție de sulfat de fier II, soluție de hidroxid de sodiu, pipetă.
Descrierea experimentului:
- Pune pe sticla de ceas câteva picături de soluție de FeSO4 și adaugă soluție de hidroxid de sodiu până la precipitarea completă
- Ce observi ?
Se formează un precipitat alb-verzui de Fe(OH)2.
Concluzia experimentului:
Cationul Fe2+ formează cu hidroxidul de sodiu, un precipitat alb-verzui de hidroxid de fier (II) :
Fe2+ + 2OH- → Fe(OH)2 ↓
FeSO4 + 2NaOH → Fe(OH)2 ↓ + Na2SO4
Hidroxidul de fier (II), la aer, își schimbă repede culoarea de la verde până la roșu-brun.
👀 Experiment: Identificarea cationului de fier II (Fe2+) cu hexacianoferatul (III) de potasiu (fericianura de potasiu), K3[Fe(CN)6]
🔥 Atenție! Hexacianoferatul (III) de potasiu este periculos pentru mediu!
Materiale necesare:
Sticlă de ceas sau eprubetă, soluție de sulfat de fier II, fericianură de potasiu (cristale roșii), pipetă.
Descrierea experimentului:
- Pune pe sticla de ceas câteva picături de soluție de FeSO4 și adaugă soluție de fericianură de potasiu până la precipitarea completă.
- Ce observi ?
Se formează un precipitat albastru de hexacianoferat (III) de fier (II).
Concluzia experimentului:
Cationul de fier II, Fe2+, formează cu hexacianoferatul (III) de potasiu (fericianura de potasiu) un precipitat de culoare albastră de hexacianoferat (III) de fier (II), cunoscut sub denumirea de 'albastru de Turnbull'.
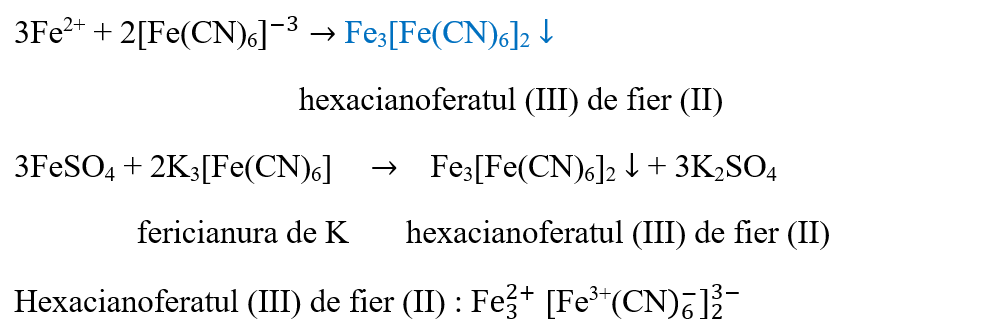
👀 Experiment: Identificarea cationului de fier III (Fe3+) cu hexacianoferat (II) de potasiu (ferocianura de potasiu), K4[Fe(CN)6]
🔥 Atenție! Hexacianoferatul (II) de potasiu este periculos pentru mediu!
Materiale necesare:
Sticlă de ceas sau eprubetă, soluție de clorură de fier III, soluție de hexacianoferat (II) de potasiu (ferocianura de potasiu), pipetă.
Descrierea experimentului:
- Pune pe sticla de ceas câteva picături de soluție de FeCl3 și adaugă soluție de hexacianoferat (II) de potasiu până la precipitarea completă. Reacţia se poate executa pe lamă de microscop sau pe hârtie de filtru.
- Ce observi ?
Se formează un precipitat albastru de hexacianoferat (II) de fier (III).
Concluzia experimentului:
Hexacianoferatul (II) de potasiu, K4[Fe(CN)6] formează cu cationul de Fe3+, un precipitat albastru amorf de hexacianoferat (II) de fier (III), cunoscut sub denumirea de “albastru de Berlin” sau “albastru de Prusia”, folosit ca pigment.

👀 Experiment: Identificarea cationului de fier III (Fe3+) cu tiocianat de potasiu (KSCN)
🔥 Atenție! Tiocianatul de potasiu este nociv, iritant și periculos pentru mediu!
Materiale necesare:
Sticlă de ceas sau eprubetă, soluție de clorură de fier III, soluție de tiocianat de potasiu (KSCN), pipetă.
Descrierea experimentului:
- Pune pe sticla de ceas câteva picături de soluție de FeCl3 și adaugă soluție de tiocianat de potasiu.
- Ce observi ?
Se formează o soluție roșu-sângeriu, de tiocianat de fier III.
Concluzia experimentului:
Tiocianatul de potasiu (sulfocianura de potasiu sau rodanura de potasiu), formează cu cationul de fier (III), o soluție roșu-sângeriu, de tiocianat de fier III:

👀 Experiment: Identificarea cationului de fier III (Fe3+) cu acetat de sodiu (CH3COONa)
🔥 Atenție! Acetatul de sodiu este nociv!
🔥 Atenție! Acetatul de fier III este caustic și iritant!
Materiale necesare:
Eprubetă, clorură de fier III, soluție de acetat de sodiu, spatulă, clește de lemn, pipetă, spirtieră.
Descrierea experimentului:
- Pune în eprubetă soluția de FeCl3 și adaugă cu pipeta soluție de acetat de sodiu CH3COONa.
- Ce observi ?
S-a format o soluție roșie de acetat de fier III.
FeCl3 + 3 CH3COONa → Fe(CH3COO)3 + 3 NaCl
- Încălzește soluția obținută până la fierbere.
- Ce observi ?
S-a format un precipitat brun de acetat bazic de fier III.