IV.1. Structura tabelului periodic al elementelor
Chimistul rus, Dimitri Mendeleev, a publicat în anul 1869 ceea ce avea să fie primul tabel periodic recunoscut la nivel mondial.

A scris pe cartonașe elementele chimice cunoscute atunci (în număr de 70), masa lor atomică și câteva proprietăți importante și le-a aranjat în ordinea creșterii masei lor atomice, punând unele sub altele pe cele cu proprietăți asemănătoare.
Iată cum era organizat Tabelul lui Mendeleev:
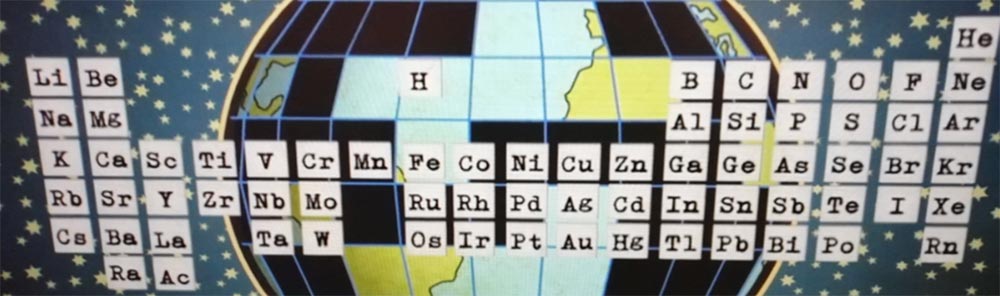
Astfel a fost realizat Tabelul periodic al elementelor, numit și Sistemul periodic al lui Mendeleev, care cuprinde într-o formă tabelară toate elementele chimice, aranjate în funcție de numărul lor atomic și unele proprietăți.
Mendeleev a prezis unele proprietăți ale elementelor încă nedescoperite, care lipseau din tabel. Majoritatea predicțiilor s-au dovedit a fi adevărate pe măsură ce noi elemente au fost descoperite. De atunci tabelul periodic al lui Mendeleev a fost dezvoltat și corectat, întrucât noi elemente au fost sintetizate sau descoperite.
Toate elementele, de la numărul atomic 1 (hidrogen) până la 118 (oganesson) au fost descoperite în natură sau obținute artificial (sintetizate). Sinteza elementelor cu un număr atomic peste 118 este planificată în viitor.
Mendeleev descoperă legea periodicității.
Legea periodicității:
Proprietățile fizice și chimice ale elementelor se repetă în mod periodic, în funcție de numărul atomic Z.
Cele 7 șiruri (orizontale) din tabel se numesc perioade. Perioadele, notate cu litere arabe de la 1 la 7, sunt șiruri (orizontale) care conțin 2,8,18 sau 32 de elemente și fiecare perioadă se termină cu un gaz rar.
Coloanele (verticale) din tabelul periodic conțin elemente ale căror atomi conțin același număr de electroni pe ultimul strat și care au proprietăți asemănătoare se numesc grupe.
Grupele sunt în număr de 18 și se clasifică în:
1. Grupe principale notate cu cifre romane urmate de litera A (IA-VIII A) sau cele cu cifre arabe 1,2,13,14,15,16,17,18 și conțin mai mult de 5 elemente.
2. Grupele secundare notate cu cifre romane urmate de litera B în număr de 10 (IB-VIIIB, ultima fiind în nr. de 3 grupe) sau cu litere arabe (3-12).
Poziția unui element chimic în Sistemul periodic este dată de perioada și de grupa în care este situat.
În tabelul periodic avem trei tipuri de substanțe simple:
-
Metale alcaline (gr.IA), alcalino-pământoase (IIA), pământoase (IIIA) și metale tranziționale (cele din grupele secundare). Ele sunt situate sub o linie îngroșată, în zigzag.
-
Nemetale separate de metale printr-o linie îngroșată, în zigzag (scăriță) și aflate deasupra liniei.
-
Gaze rare situate în grupa VIII A: He, Ne, Ar, Kr, Xe, Rn.
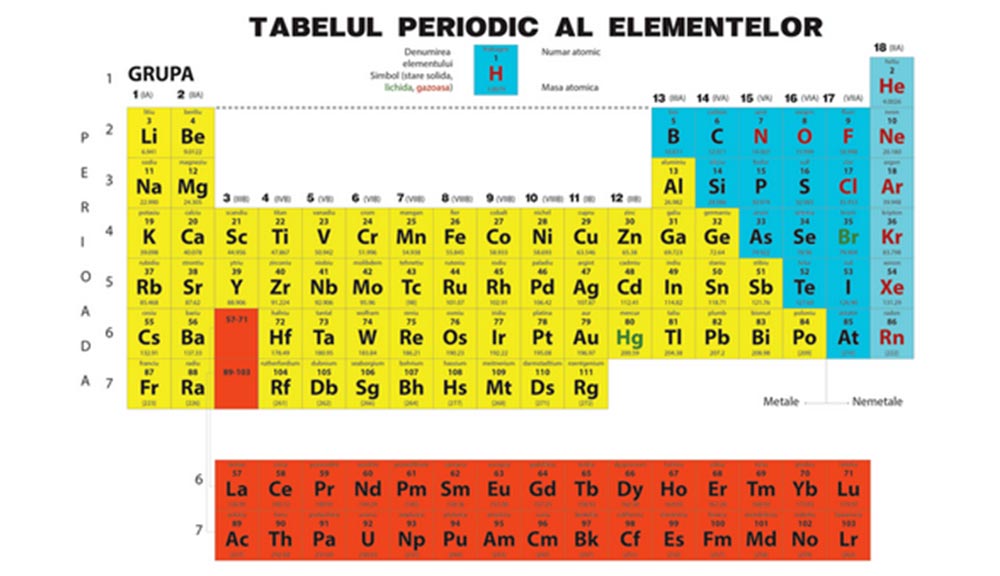
Observă Tabelul periodic și răspunde la următoarele întrebări :
1. Care dintre elementele H, Cu, Mg, C, I, Na fac parte din perioada a 3-a?
2. Care este legea după care s-a stabilit poziția elementelor în acest Tabel?
3. Denumește metalele alcaline și nemetalele din grupa a VII A .
4. Care este poziția în Sistemul periodic al următoarelor elemente: H, K, O, Al, F, Cu ?
5. Completează spațiile libere:
a) Savantul rus Mendeleev aranjează unele sub altele elemente cu ..................................................
b) Același șir (orizontal) cuprinde elementele chimice în ordinea crescătoare a ...................................
c) Tabelul periodic conține ...... coloane, numite................... și ...... șiruri, numite ...................