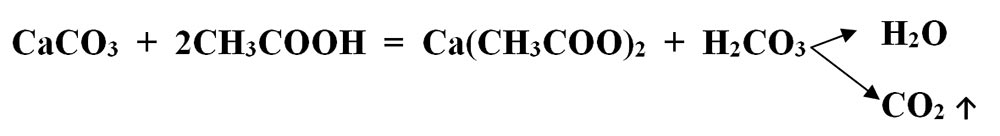VI.6. Reacția acizilor cu sărurile
🔥 Atenție! Acest experiment se efectuează numai de către profesori!
🔥 Atenție! Azotatul de argint și acidul clorhidric sunt caustice și îți pot produce arsuri în contact cu pielea !
Materiale necesare:
Sticlă de ceas sau eprubetă, acid clorhidric, soluție de azotat de argint (piatra iadului), pipetă.
Descrierea experimentului:
- Pune în sticla de ceas câteva picături de acid clorhidric și adaugă apoi puțină soluție de azotat de argint.
- Ce observi ?
S-a format un precipitat alb.
Concluzia experimentului:
Acidul clorhidric - HCl reacționează cu azotatul de argint – AgNO3 și se transformă în clorură de argint
AgCl și acid azotic.
Este o reacție de schimb, deoarece avem ca reactanți două substanțe compuse, iar ca produși avem tot două substanțe compuse:
HCl + AgNO3 = AgCl ↓ + HNO3
🔥 Atenție! Acest experiment se efectuează numai de către profesori!
🔥 Atenție! Acidul clorhidric este caustic și îți poate produce arsuri în contact cu pielea !
Materiale necesare:
Eprubetă, soluție de sulfat de cupru (piatră vânătă), acid clorhidric, pipetă.
Descrierea experimentului:
- Pune în eprubetă puțină soluție de sulfat de cupru și adaugă câteva picături de acid clorhidric.
- Ce observi ?
Soluția albastră s-a colorat în verde.
Concluzia experimentului:
Sulfatul de cupru II – CuSO4 reacționează cu acidul clorhidric - HCl și se transformă în clorură de
cupru II - CuCl2 și acid sulfuric.
Este o reacție de schimb, deoarece avem ca reactanți două substanțe compuse, iar ca produși avem tot două substanțe compuse:
CuSO4 + 2 HCl = CuCl2 + H2SO4
🔥 Atenție! Experimentul se efectuează numai de către profesor și sub nișă sau în aer liber!
🔥 Atenție! Acetatul de plumb este toxic și periculos pentru mediu acvatic !
🔥 Atenție! Acidul sulfhidric este extrem de toxic și iritant! Provoacă arsuri grave ale căilor respiratorii, ochilor și pielii! Concentrațiile mari pot cauza pierderea conștienței și decesul imediat.
Materiale necesare:
Eprubetă, sulfură de fier, acid clorhidric, pipetă, clește de lemn, soluție de acetat de plumb, hârtie de filtru.
Descrierea experimentului:
- Pune în eprubetă sulfură de fier și câteva picături de HCl.
- Ce observi ?
Se degajă un gaz incolor cu miros de ouă clocite.
Concluzia experimentului:
Anionul sulfură în reacție cu un acid se recunoaște după degajarea acidului sulfhidric, un gaz incolor cu miros de ouă clocite.
FeS (s) + 2 HCl (aq) → FeCl2 (aq) + H2S ↓
Anionul sulfură este anionul acidului sulfhidric, care reprezintă o soluție apoasă a gazului incolor H2S, cu miros de ouă alterate, foarte toxic. Acidul sulfhidric este acid bibazic foarte slab și reducător puternic. Majoritatea sărurilor lui sunt greu solubile în apă, cu excepția sulfurile metalelor alcaline, alcalino-pământoase și cea de amoniu.
Degajarea acidului sulfhidric se recunoaște după înnegrirea hârtiei de filtru îmbibată cu soluție de acetat de plumb:
H2S (g) + (CH3COO)2Pb (aq) → 2 CH3COOH (aq) + PbS ↓
🔥 Atenție! Acest experiment se efectuează numai de către profesori!
🔥 Atenție! Acidul sulfuric este caustic și îți poate produce arsuri în contact cu pielea !
🔥 Atenție! Clorura de bariu este toxică !
Materiale necesare: creuzet, soluție de clorură de bariu, acid sulfuric, pipetă.
Descrierea experimentului:
- Pune în creuzet puțină soluție de acid sulfuric și adaugă câteva picături de clorură de bariu.
- Ce observi ?
S-a format un precipitat alb.
Concluzia experimentului:
Clorura de bariu – BaCl2 reacționează cu acidul sulfuric - H2SO4 și se transformă
în acid clorhidric – HCl și sulfat de bariu - BaSO4 (precipitat alb). Această reacție este folosită în
laborator pentru recunoașterea acidului sulfuric și a sărurilor lui, sulfați.
Este o reacție de schimb, deoarece avem ca reactanți două substanțe compuse, iar ca produși avem tot două substanțe compuse:
BaCl2 + H2SO4 = 2 HCl + BaSO4 ↓
🔥 Atenție! Acest experiment se efectuează numai de către profesori!
🔥 Atenție! Acidul sulfuric este caustic și îți poate produce arsuri în contact cu pielea !
Materiale necesare: eprubetă, carbonat de sodiu, soluție de acid sulfuric, pipetă, chibrit.
Descrierea experimentului:
- Pune în eprubetă puțin carbonat de sodiu (praf de copt) și adaugă câteva picături de acid sulfuric (poți adăuga și oțet, care este un acid organic).
- Vino deasupra eprubetei cu un băț de chibrit aprins.
- Ce observi ?
Reacția este efervescentă și gazul rezultat stinge bățul de chibrit.
Concluzia experimentului:
Carbonatul de sodiu – Na2CO3 reacționează cu acidul sulfuric - H2SO4 și se transformă în sulfat de sodiu – Na2SO4 și acid carbonic - H2CO3, care este instabil și se descompune în apă și dioxid de carbon –CO2 , care stinge flacăra chibritului. Reacția dintre un carbonat și un acid este folosită în laborator pentru recunoașterea carbonaților.
Este o reacție de schimb, deoarece avem ca reactanți două substanțe compuse, iar ca produși avem tot două substanțe compuse:
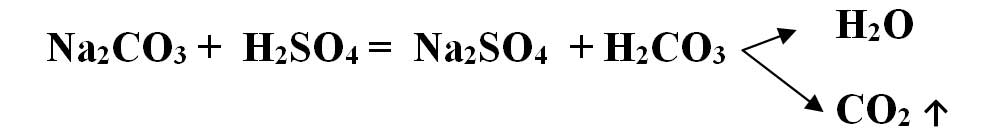
Materiale necesare:
Pahar, oțet (soluție de acid acetic), un ou crud.
Descrierea experimentului:
- Pune în pahar un ou crud și adaugă peste el oțet, cât să îl acopere. Reacția este extrem de lentă. Ține sub observație oul până când acesta rămâne fără coajă.
- Ce observi ?
Imediat când punem oul în oțet, încep să iasă niște bule din coaja acestuia. După o zi oul a rămas fără coajă și privit în lumină a devenit translucid.
Concluzia experimentului:
Carbonatul de calciu – CaCO3 (componentul principal al cojii de ou) reacționează cu acidul acetic
din oțet- CH3COOH și se transformă în acetat de calciu – Ca(CH3COO)2 și acid
carbonic - H2CO3, care este instabil și se descompune în apă și dioxid de carbon – CO2.
Este o reacție de schimb, deoarece avem ca reactanți două substanțe compuse, iar ca produși avem tot două substanțe compuse: