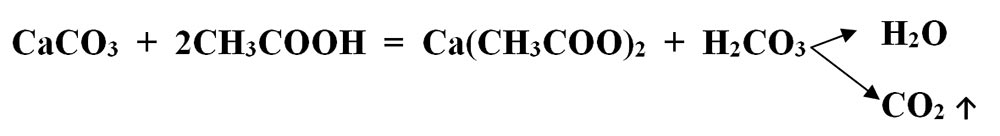VI.6. Reacția acizilor cu sărurile
🔥 Atenție! Acest experiment se efectuează numai de către profesori!
🔥 Atenție! Azotatul de argint și acidul clorhidric sunt caustice și îți pot produce arsuri în contact cu pielea !
Materiale necesare:
Sticlă de ceas sau eprubetă, acid clorhidric, soluție de azotat de argint (piatra iadului), pipetă.
Descrierea experimentului:
- Pune în sticla de ceas câteva picături de acid clorhidric și adaugă apoi puțină soluție de azotat de argint.
- Ce observi ?
S-a format un precipitat alb.
Concluzia experimentului:
Acidul clorhidric - HCl reacționează cu azotatul de argint – AgNO3 și se transformă în clorură de argint
AgCl și acid azotic.
Este o reacție de schimb, deoarece avem ca reactanți două substanțe compuse, iar ca produși avem tot două substanțe compuse:
HCl + AgNO3 = AgCl ↓ + HNO3
🔥 Atenție! Acest experiment se efectuează numai de către profesori!
🔥 Atenție! Acidul clorhidric este caustic și îți poate produce arsuri în contact cu pielea !
Materiale necesare:
Eprubetă, soluție de sulfat de cupru (piatră vânătă), acid clorhidric, pipetă.
Descrierea experimentului:
- Pune în eprubetă puțină soluție de sulfat de cupru și adaugă câteva picături de acid clorhidric.
- Ce observi ?
Soluția albastră s-a colorat în verde.
Concluzia experimentului:
Sulfatul de cupru II – CuSO4 reacționează cu acidul clorhidric - HCl și se transformă în clorură de
cupru II - CuCl2 și acid sulfuric.
Este o reacție de schimb, deoarece avem ca reactanți două substanțe compuse, iar ca produși avem tot două substanțe compuse:
CuSO4 + 2 HCl = CuCl2 + H2SO4
🔥 Atenție! Acest experiment se efectuează numai de către profesori!
🔥 Atenție! Acidul sulfuric este caustic și îți poate produce arsuri în contact cu pielea !
🔥 Atenție! Clorura de bariu este toxică !
Materiale necesare: creuzet, soluție de clorură de bariu, acid sulfuric, pipetă.
Descrierea experimentului:
- Pune în creuzet puțină soluție de acid sulfuric și adaugă câteva picături de clorură de bariu.
- Ce observi ?
S-a format un precipitat alb.
Concluzia experimentului:
Clorura de bariu – BaCl2 reacționează cu acidul sulfuric - H2SO4 și se transformă
în acid clorhidric – HCl și sulfat de bariu - BaSO4 (precipitat alb). Această reacție este folosită în
laborator pentru recunoașterea acidului sulfuric și a sărurilor lui, sulfați.
Este o reacție de schimb, deoarece avem ca reactanți două substanțe compuse, iar ca produși avem tot două substanțe compuse:
BaCl2 + H2SO4 = 2 HCl + BaSO4 ↓
🔥 Atenție! Acest experiment se efectuează numai de către profesori!
🔥 Atenție! Acidul sulfuric este caustic și îți poate produce arsuri în contact cu pielea !
Materiale necesare: eprubetă, carbonat de sodiu, soluție de acid sulfuric, pipetă, chibrit.
Descrierea experimentului:
- Pune în eprubetă puțin carbonat de sodiu (praf de copt) și adaugă câteva picături de acid sulfuric (poți adăuga și oțet, care este un acid organic).
- Vino deasupra eprubetei cu un băț de chibrit aprins.
- Ce observi ?
Reacția este efervescentă și gazul rezultat stinge bățul de chibrit.
Concluzia experimentului:
Carbonatul de sodiu – Na2CO3 reacționează cu acidul sulfuric - H2SO4 și se transformă în sulfat de sodiu – Na2SO4 și acid carbonic - H2CO3, care este instabil și se descompune în apă și dioxid de carbon –CO2 , care stinge flacăra chibritului. Reacția dintre un carbonat și un acid este folosită în laborator pentru recunoașterea carbonaților.
Este o reacție de schimb, deoarece avem ca reactanți două substanțe compuse, iar ca produși avem tot două substanțe compuse:
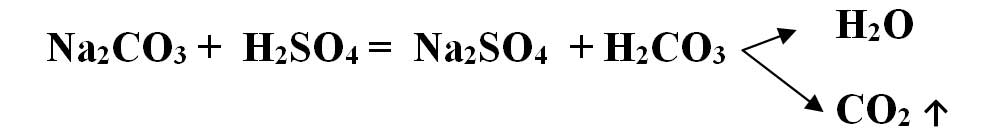
Materiale necesare:
Pahar, oțet (soluție de acid acetic), un ou crud.
Descrierea experimentului:
- Pune în pahar un ou crud și adaugă peste el oțet, cât să îl acopere. Reacția este extrem de lentă. Ține sub observație oul până când acesta rămâne fără coajă.
- Ce observi ?
Imediat când punem oul în oțet, încep să iasă niște bule din coaja acestuia. După o zi oul a rămas fără coajă și privit în lumină a devenit translucid.
Concluzia experimentului:
Carbonatul de calciu – CaCO3 (componentul principal al cojii de ou) reacționează cu acidul acetic
din oțet- CH3COOH și se transformă în acetat de calciu – Ca(CH3COO)2 și acid
carbonic - H2CO3, care este instabil și se descompune în apă și dioxid de carbon – CO2.
Este o reacție de schimb, deoarece avem ca reactanți două substanțe compuse, iar ca produși avem tot două substanțe compuse: