VII.3.1. Principiul lui Le Châtelier.
Pentru o reacție reversibilă, starea de echilibru chimic se stabilește atunci când concentrația componentelor rămâne constantă, iar temperatura și presiunea sistemului nu se modifică.
Principiul lui Le Châtelier explică ce se întâmplă cu sistemul aflat în echilibru chimic atunci când se modifică condițiile experimentale : concentrația componentelor, temperatura sau presiunea.
🔦 Observație
Catalizatorii nu deplasează echilibrul chimic, ci grăbesc atingerea acestuia.
Catalizatorii cresc viteza de reacție, atât a reacției directe, cât și a celei inverse (proprietatea nr. 1 a catalizatorilor).
Catalizatorii nu se consumă în timpul reacțiilor, dar acest lucru nu înseamnă neparticiparea lor la reacție (proprietatea nr. 2 a catalizatorilor).
Prezența catalizatorului determină un ciclu de procese la sfârșitul căruia catalizatorul apare în forma lui inițială.
Principiul lui Le Châtelier:
Orice modificare aplicată unui sistem în echilibru deplasează echilibrul în sensul diminuării modificării respective.
Factorii care influențează echilibrul chimic sunt: modificarea concentrației unui component, modificarea temperaturii sistemului și modificarea presiunii sistemului.
👀 Experiment: Principiul lui Le Châtelier.
🔥 Atenție! Acidul clorhidric concentrat este extrem de caustic!
🔥 Atenție! Clorura de cobalt este toxică, extrem de iritantă și periculoasă pentru mediul acvatic!
Materiale necesare:
2 pahare Berzelius, soluție de clorură de cobalt II hexahidratată, apă distilată, HCl concentrat, apă fiartă, apă cu gheață, pipetă.
Mod de lucru:
-
Prepară o soluție de CoCl2. Observă culoarea acesteia.
Soluția de clorură de cobalt II hexahidratată are o culoare roșu-vișiniu datorită ionilor de cobalt hexahidratați, [Co(H2O)6]+2. Spunem că există un echilibru între moleculele nedisociate și cationii de cobalt hexahidratați.
În acest caz viteza reacției directe (cea de la stânga la dreapta) este egală cu viteza reacției inverse (cea de la dreapta la stânga) și concentrațiile reactanților și a produșilor de reacție rămân constante.
CoCl2 + 6 HOH ⇄ [Co(H2O)6]+2 + 2 Cl-
- Adaugă câteva picături de acid clorhidric concentrat. Încălzește eprubeta în apă caldă până când soluția devine albastră.
Conform principiul lui Le Châtelier, orice modificare aplicată unui sistem în echilibru deplasează echilibrul în sensul diminuării modificării respective.
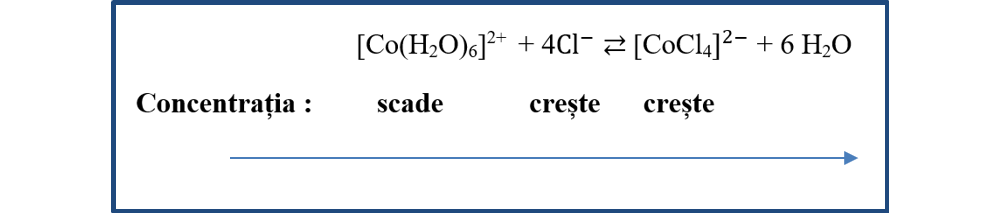
La adăugarea unui ion comun (Cl-) soluției, ionii clorură înlocuiesc moleculele de apă din jurul ionului de cobalt, cu formarea unor ioni complecși de tetraclorocobaltat II. Astfel creștem concentrația anionilor de clor care va produce și creșterea concentrației ionului complex de tetraclorocobaltat, de culoare albastră. Echilibrul se va deplasa spre dreapta, în sensul consumării componentului respectiv (Cl-).
- Adaugă apă până când soluția devine roșie.
La adăugarea de apă soluției, creștem concentrația apei astfel încât se va produce și creșterea concentrației cationilor de cobalt hexahidratați, de culoare roșu-vișiniu. Echilibrul se va deplasa spre stânga, în sensul consumării componentului respectiv (H2O).

- • Pune eprubeta cu soluție roșu-vișiniu într-un pahar cu apă cu gheață.
- Ce observi?
Soluția din eprubeta cu gheață a căpătat o culoare roz.
Concluzia experimentului:
La creșterea temperaturii este favorizată reacția endotermă (reacția care are loc cu absorbție de căldură), echilibrul fiind deplasat spre dreapta cu creșterea concentrației ionului complex de tetraclorocobaltat, de culoare albastră.
La scăderea temperaturii este favorizată reacția exotermă (reacția care are loc cu degajare de căldură), echilibrul fiind deplasat spre stânga cu creșterea concentrației cationilor de cobalt hexahidratați, de culoare roz.
