VI.2.3.6. Identificarea cationului de cobalt
👀 Experiment: Identificarea cationului de cobalt II (Co2+) cu hidroxid de sodiu
🔥 Atenție! Clorura de cobalt este toxică, extrem de iritantă și periculoasă pentru mediul acvatic!
🔥 Atenție! Hidroxidul de sodiu este caustic !
Materiale necesare:
Eprubetă, soluție de clorură de cobalt II, soluție de hidroxid de sodiu, pipetă, spirtieră, clește de lemn.
Descrierea experimentului:
- Pune pe sticla de ceas câteva picături de soluție de CoCl2 și adaugă soluție diluată de hidroxid de sodiu până la precipitarea completă.
- Ce observi ?
S-a format un precipitat albastru.
CoCl2 + NaOH → CoOHCl ↓ + NaCl
Corură de cobalt II + hidroxid de sodiu → Clorură bazică de cobalt II + Clorură de sodiu
- Adaugă peste precipitatul de clorură bazică de cobalt II câteva picături de hidroxid de sodiu și încălzește ușor.
- Ce observi ?
Precipitatul albastru de clorură bazică de cobalt II își schimbă culoarea în roz.
CoOHCl ↓ + NaOH → Co(OH)2↓ + NaCl
Clorură bazică de cobalt II + Hidroxid de sodiu → Hidroxid de cobalt II
- Adaugă în precipitatul roz de hidroxid de cobalt II câteva picături de apă oxigenată
- Ce observi ?
Culoarea roz se schimbă în brună.
2 Co(OH)2↓ + H2O2 → 2 Co(OH)3 ↓
Hidroxid de cobalt II + Apă oxigenată → Hidroxid ce cobalt III
Concluzia experimentului:
Bazele alcaline formează cu ionii de cobalt II sarea bazică de cobalt, precipitat de culoare albastră, care în exces de reactiv, la încălzire, se transformă în hidroxid de cobalt II, de culoare roz.
Hidroxidul de cobalt II în contact cu oxigenul din aer și treptat sau la adăugarea de apă oxigenată, se transformă în hidroxid de cobalt III, de culoare brună. Acesta nu este solubil în acid sulfuric, dar se dizolvă în amestecul acestuia cu apa oxigenată.
Poți efectua acestă reacție și sub o picătură de apă pusă pe o monedă în care să introduci cu un ac un cristal de clorură de cobalt hexahidratată și apoi un cristal de hidroxid de sodiu. După formarea precipitatului albastru de clorură bazică de cobalt II, încălzește-l. După formarea precipitatului roz de carbonat de cobalt II adaugă 1-2 picături de apă oxigenată concentrată. Se formează un precipitat brun de carbonat de cobalt III.
👀 Experiment: Identificarea cationului de cobalt II (Co2+) cu hexacianoferat (III) de potasiu
🔥 Atenție! Hexacianoferatul (III) de potasiu este toxic și periculos pentru mediu!
Materiale necesare:
Sticlă de ceas sau eprubetă, soluție de clorură de cobalt II, soluție de hexacianoferat (III) de potasiu, pipetă.
Descrierea experimentului:
- Pune pe sticla de ceas câteva picături de soluție de CoCl2 și adaugă soluție de hexacianoferat (III) de potasiu până la precipitarea completă.
- Ce observi ?
Se formează un precipitat verde de hexacianoferat (II) de cobalt (II).
Concluzia experimentului:
Hexacianoferatul (III) de potasiu (fericianura ce potasiu), K3[Fe(CN)6], formează cu cationul de Co2+, un precipitat verde de hexacianoferat (II) de cobalt (II).
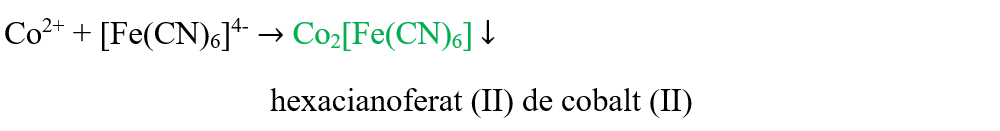
👀 Experiment: Identificarea cationului de cobalt II (Co2+) cu amoniac
🔥 Atenție! Clorura de cobalt este toxică, extrem de iritantă și periculoasă pentru mediul acvatic!
🔥 Atenție! Soluția de amoniac este foarte toxică, corozivă, extrem de iritantă și periculoasă pentru mediu!
Materiale necesare:
Sticlă de ceas, soluție de clorură de cobalt II, soluție de amoniac diluată și concentrată, pipetă.
Descrierea experimentului:
- Pune pe sticla de ceas câteva picături de soluție de CoCl2 și adaugă tot 3 picături de soluție diluată de amoniac până la precipitarea completă
- Ce observi ?
S-a format un precipitat albastru-verzui.
- Peste precipitatul obținut adaugă soluție concentrată de amoniac până la dizolvarea completă a precipitatului.
- Ce observi ?
S-a format o soluție galben-cenușie.
Concluzia experimentului:
Soluția apoasă de amoniac (hidroxid de amoniu) precipită cationul de Co+2 cu formarea de clorură bazică de cobalt II. La acțiunea cu exces de amoniac (soluție concentrată de amoniac) precipitatul se dizolvă cu formare de compuși coordinativi.
CoCl2 + NH4OH (dil.) → CoOHCl ↓ + NH4Cl
Clorură de cobalt II + hidroxid de amoniu → clorură bazică de cobalt II + clorură de amoniu
CoOHCl ↓ + NH4Cl + 5 NH4OH → [Co(NH3)6]Cl2 + 6 H2O
clorură bazică de cobalt II + clorură de amoniu + hidroxid de amoniu (conc.) → Diclorohexaaminocobalt II + apă
👀 Experiment: Identificarea cationului de cobalt II (Co2+) cu carbonatul de sodiu
🔥 Atenție! Clorura de cobalt este toxică, extrem de iritantă și periculoasă pentru mediul acvatic!
Materiale necesare:
Sticlă de ceas, soluție de clorură de cobalt II, soluție de carbonat de sodiu, pipetă.
Descrierea experimentului:
- Pune pe sticla de ceas câteva picături de soluție de CoCl2 și adaugă soluție de carbonat de sodiu până la precipitarea completă.
- Amestecă ușor.
- Ce observi ?
S-a format un precipitat roz-violet.
Concluzia experimentului:
Carbonatul de sodiu precipită din clorura de cobalt II carbonatul de cobalt II, de culoare roz-violet.
Reacția dintre clorura de cobalt II și carbonatul de sodiu este o reacție de dublu schimb (precipitare) care produce un precipitat roz-violet de carbonat de cobalt II și clorură de sodiu.
CoCl2 (aq) + Na2CO3 (aq) → CoCO3 ↓ + 2NaCl (aq)
👀 Experiment: Identificarea cationului de cobalt II (Co2+) cu hexacianoferatul II de potasiu
🔥 Atenție! Clorura de cobalt este toxică, extrem de iritantă și periculoasă pentru mediul acvatic!
🔥 Atenție! Hexacianoferatul (II) de potasiu este periculos pentru mediu!
Materiale necesare:
Sticlă de ceas, soluție de clorură de cobalt II, soluție de hexacianoferatul (II) de potasiu, pipetă.
Descrierea experimentului:
- Pune pe sticla de ceas câteva picături de soluție de CoCl2 și adaugă soluție de hexacianoferatul (II) de potasiu până la precipitarea completă.
- Amestecă ușor.
- Ce observi ?
S-a format un precipitat verde-măsliniu.
Concluzia experimentului:
Hexacianoferatul (II) de potasiu precipită din clorura de cobalt II hexacianoferatul (II) de cobalt II, de culoare verde-măsliniu .
2 CoCl2 (aq) + K4[Fe(CN)6] (aq)→ Co2[Fe(CN)6] (s)↓ + 4 KCl (aq)