II.1. Substanțe pure și amestecuri de substanțe
Substanța pură are o compoziție bine determinată, are constante fizice specifice și își păstrează compoziția în urma unor fenomene fizice.
Materiale necesare:
2 pahare Berzelius, apă, baghetă de sticlă, sare extrafină și sare grunjoasă.
Descrierea experimentului:
- Pune într-un pahar sarea extrafină și în celălalt sarea grunjoasă.
- Adaugă apă în ambele pahare și dizolvă sarea prin agitarea cu bagheta și apoi observă conținuturile celor 2 pahare.
- Ce observi ?
În paharul cu apă și sare fină nu se deosebesc componenții, iar în celălalt se depun pe fund substanțe închise la culoare.
Concluzia experimentului:
Sarea fină este o substanță pură, iar sarea grunjoasă este impură adică, conține impurități (alte substanțe pe lângă
sare).
Pentru a exprima cât de curată este o substanță se folosește noțiunea de puritate.
Puritatea (p) reprezintă masa de substanță pură care se găsește în 100 g de substanță impură. Ea se exprimă în procente (%).
1. Din 800 g sare grunjoasă se obține 700 g sare pură. Calculați puritatea zăcământului și procentul impurităților.
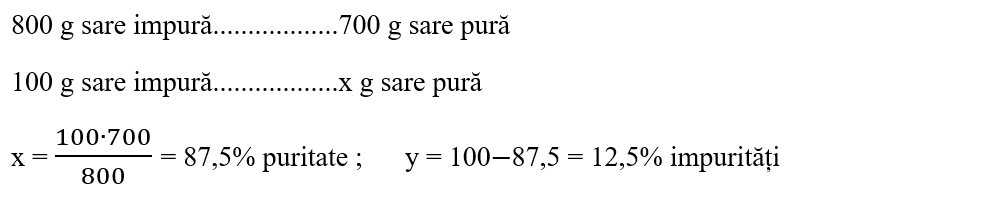
Amestecul este rezultatul punerii în comun a două sau mai multe substanțe între care nu au loc fenomene chimice (reacții chimice).
Zilnic folosești amestecuri sub diferite forme: preparate culinare, medicamente, pastă de dinți, detergenți, produse cosmetice etc.
🔥 Atenție! Acest experiment se efectuează numai de către profesori!
🔥 Atenție! Mercurul este extrem de toxic ! Nu inhala vaporii săi! Nu îl atinge și nu il gusta!
Materiale necesare:
Mojar cu pistil, sulf, pilitură de fier, o picătură de mercur, magnet.
Descrierea experimentului:
-
Pune într-un mojar pulbere de sulf și pilitură de fier și amestecă totul cu pistilul.
-
Apropie de acest amestec un magnet.
-
Ce observi ?
Fierul din amestec nu își pierde proprietatea de a fi atras de magnet.
Sulful din amestec își păstrează și el proprietățile (pulbere galbenă). -
Pune într-un mojar pulbere de sulf și o picătură de mercur și amestecă totul cu pistilul.
-
Ce observi ?
În scurt timp vei observa o pulbere neagră și formarea unei noi substanțe care nu mai are proprietățile celor 2 componente.
Concluzia experimentului:
Sulful cu fierul amestecate în mojar formează un amestec.
Sulful cu mercurul suferă un fenomen chimic, în urma căruia cele două substanțe nu își mai păstrează proprietățile.
Caracteristicile amestecurilor
A) Un amestec este format din doi sau mai mulți componenți.
B) Substanțele componente pot fi luate în diferite proporții.
C) Fiecare substanță componentă își păstrează proprietățile fizice și chimice.
Un amestec poate fi format din:
- Substanțe solide: solul, rocile, aliajele
- Substanțe lichide: diverse băuturi, antigelul
- Substanțe gazoase: aerul, gazele naturale
- Substanțe în cele 3 stări de agregare: apa tulbure (apă + particule solide + aer dizolvat)
Obținerea amestecurilor:
a) Amestecarea componenților în stare gazoasă are loc de la sine prin fenomenul de difuzie, datorat mișcării dezordonate și continue a particulelor componente.
b) Amestecarea unui lichid cu:
- un gaz prin barbotarea (suflarea) gazului în lichid;
- alt lichid, tot de la sine prin difuzie;
- un solid, prin amestecare și dizolvare.
c) Amestecarea componenților în stare solidă cu ajutorul mojarului cu pistil.
După compoziția lor amestecurile se clasifică în:
1. Amestecuri omogene care au aceeași compoziție și aceleași proprietăți în toată masa lor.
Exemple de amestecuri omogene:
- soluții;
- aliaje;
- oțet;
- aer;
- spirt.

2. Amestecuri eterogene care nu au aceeași compoziție și aceleași proprietăți în toată masa lor și se observă cu ochiul liber sau cu lupa componenții săi.
Exemple de amestecuri eterogene:
- apă cu ulei;
- apă cu nisip;
- aer cu mercur;
- preparate culinare;
- roci etc.

Materiale necesare:
Bobițe din folie de aluminiu, praf de cretă, griș, cerneală (albastru de metilen), sare de lămâie, piper, petrol,
zaț de cafea, bicarbonat de sodiu, pahare transparente.
Descrierea experimentului:
- În fiecare pahar pune puțină apă (10 mL). Adaugă în fiecare diferitele substanțe pe care le ai în casă (prezentate la materiale necesare sau altele). Amestecă atent conținutul fiecărui pahar.
- Analizează aspectul fiecărui amestec și observă cu ochiul liber dacă au aceeași compoziție și aceleași proprietăți în toată masa lor.
- Completează următorul tabel în care să scrii ce fel de amestec este fiecare.
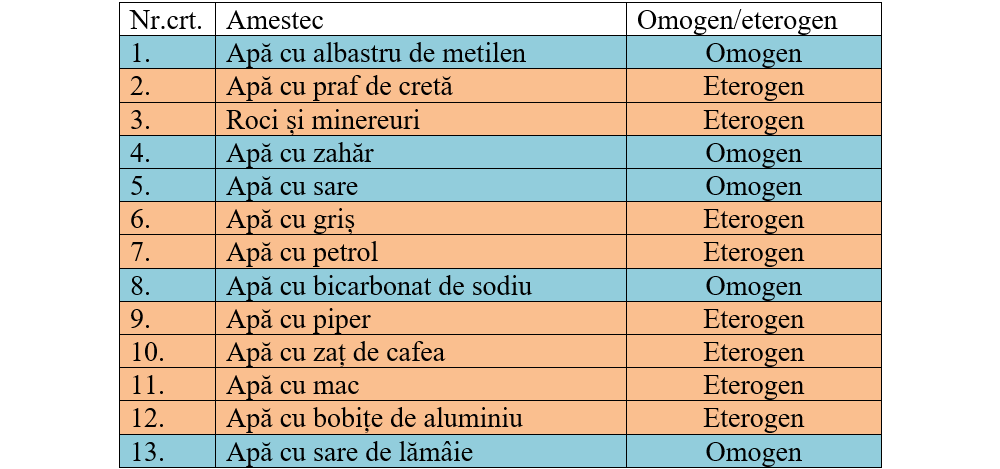
Concluzia experimentului:
În cazul în care o substanță se dizolvă în altă substanță se formează o soluție, care este un amestec omogen.
Amestecul omogen are aceeași compoziție și aceleași proprietăți în toată masa lui.
Amestecul eterogen nu are aceeași compoziție și aceleași proprietăți în toată masa lui (se observă cu ochiul liber
sau cu microscopul componenții lui).
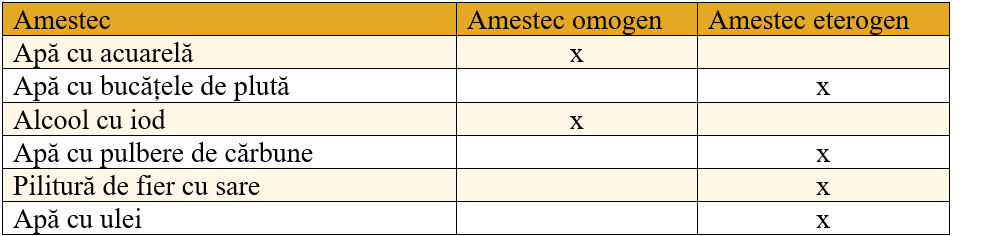
1. Dă câte 3 exemple de substanțe pure, amestecuri omogene și eterogene.

2. Identifică tipul de amestec din tabel.