III.2. Caracterul metalic și electropozitiv.
În natură marea majoritate a substanțelor se găsesc sub formă de compuși chimici.
Elementele chimice care se găsesc sub formă de atomi liberi stabili sunt cele șase gaze nobile (rare) din grupa a VIII a A (sau grupa nr.18) a Tabelului periodic: Heliu (He), Neon (Ne), Argon (Ar), Kripton (Kr), Xenon (Xe) și Radon (Rn), având configurație stabilă a ultimului strat de dublet (He) sau octet (celelalte gaze rare).
Atomii celorlalte elemente se unesc între ei pentru a obține forme stabile, ioni sau molecule.
Atomii metalelor, având un număr mic de electroni pe ultimul strat, cedează acești electroni și ajung la configurația stabilă a penultimului strat, identică cu cea a gazului rar precedent lui în Sistemul periodic.
Prin cedare de electroni atomii metalelor devin ioni pozitivi (cationi), deoarece vor avea un surplus de protoni în nucleu. Spunem că metalele au un caracter electropozitiv.
Formarea ionilor pozitivi:
M - n ē → M+n (Ion pozitiv sau cation)
unde M = metal, n = nr electroni cedați = sarcina ionului

- Metalele din grupa a 2 a (a II-a A) au 2 ē de valență pe care îi cedează, formând ioni pozitivi cu sarcina +2.

- Metalele din grupa a 13 a (a III-a A) au 3 ē de valență pe care îi cedează, formând ioni pozitivi cu sarcina +3.
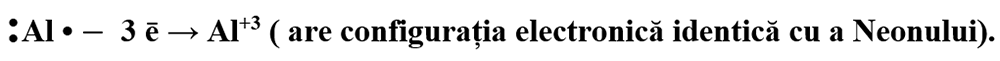
Ușurința cu care un atom poate să cedeze un electron este măsurată prin energia de ionizare pe care atomul o absoarbe pentru a deveni ion pozitiv.
Energia de ionizare reprezintă cantitatea de energie absorbită la cedarea unui electron dintr-un atom în stare gazoasă.
Energia de ionizare primară (I1) este energia absorbită în procesul de îndepărtare a electronului cel mai slab legat din atom.
E(g) + I1 → E(g)+ + ē
Energia de ionizare secundară (I2) este energia absorbită în procesul de îndepărtare a electronului din cationul E+ și așa mai departe.
E(g)+ + I2 → E(g)2+ + ē
E(g)2+ + I3 → E(g)3+ + ē
🔦 Observație
Energiile de ionizare cresc în ordinea I1 < I2 < I3 pentru că se absoarbe mai multă energie pentru a îndepărta electroni dintr-un ion pozitiv (atracția nucleului este mai mare).
Energiile de ionizare se măsoară în kJ/mol, kcal/mol sau în electronvolt (1eV = 96,49 kJ/mol).
Energia de ionizare variază periodic astfel:
- În perioadă, energia de ionizare crește de la grupa 1 la grupa 18, datorită creșterii numărului de protoni din nucleu (crește și atracția nucleului față de electroni). Cele mai mari energii de ionizare le au gazele rare.
De exemplu în perioada a 3-a:

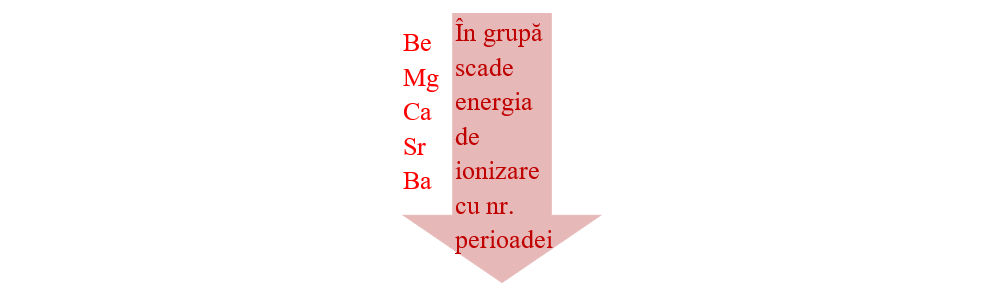
- În grupă, energia de ionizare scade de sus în jos, deoarece scade și atracția nucleului față de electronii periferici (crește distanța dintre nucleu și electronii de valență).
De exemplu în grupa a II A:
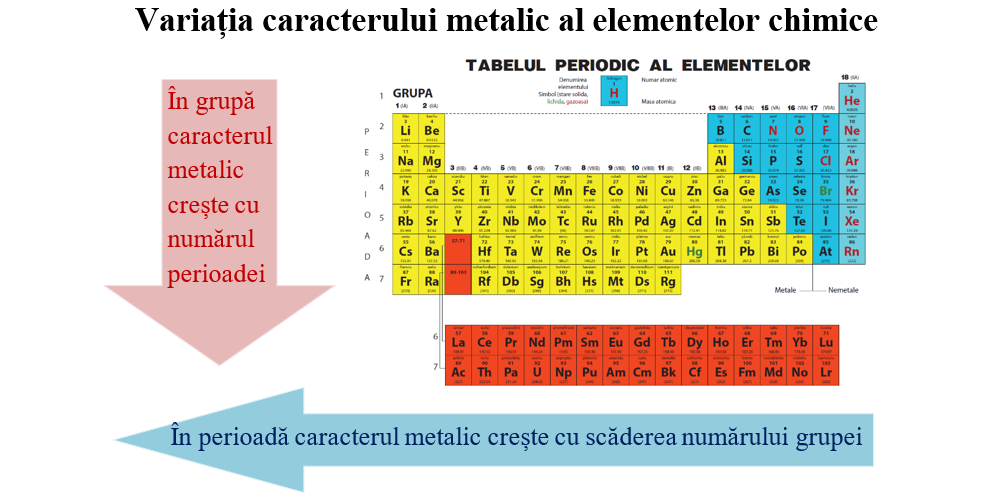
Metalele au caracter chimic metalic și caracter electrochimic electropozitiv (formează ioni pozitivi prin cedare de electroni).
Caracterul metalic crește odată cu scăderea energiei de ionizare și variază periodic în funcție de distanța electronilor de valență față de nucleu și de numărul electronilor cedați.
🔦 Observație
Cesiul (Cs) are cel mai pronunțat caracter metalic și este cel mai electropozitiv metal.
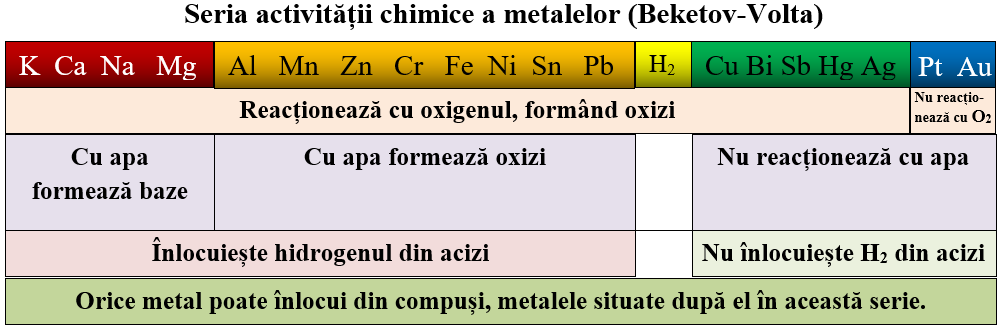
Seria activității chimice a metalelor (Beketov-Volta) constituie o clasificare a metalelor după caracterul lor electrochimic, astfel metalele sunt așezate în ordinea descrescătoare a caracterului lor metalic și, implicit, a reactivităţii lor.
Cu cât metalul este așezat mai la începutul seriei de activitate, cu atât el cedează mai ușor electronii de valență, trecând la ionul corespunzător și, deci, este mai reactiv din punct de vedere chimic.
🔦 Observație
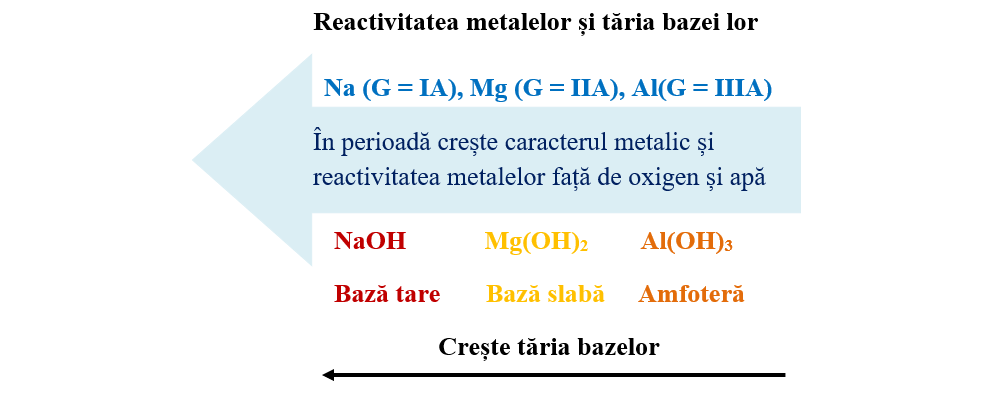
Caracterul metalic influențează nu numai reactivitatea elementelor, ci și proprietățile compușilor lor (de exemplu tăria bazelor).
👀 Experimente
Pentru a înțelege cum scade reactivitatea metalelor în acestă serie să vedem diferite experimente cu reacții de substituție.
I. Reacția de ardere are loc diferit la metale:
- Sodiul reacționează violent și la rece cu oxigenul din aer (din acest motiv se păstrează sub petrol).
- Magneziul sub formă de bandă reacționează la cald cu oxigenul, cu o flacără orbitoare.
- Aluminiul sub formă de bandă nu reacționează cu oxigenul (el se acoperă cu un strat de oxid de aluminiu). Sub formă de pulbere, aluminiul reacționează la cald cu oxigenul, cu scântei.
II. Reacția cu apa are loc diferit la metale:
- Sodiul reacționează energic (chiar violent) și la rece
- Magneziul trebuie încălzit pentru a reacționa cu apa.
- Aluminiul nu reacționează cu apa.
III. Reacția metalelor cu săruri poate avea loc numai între un metal și sărurile metalelor aflate după el în Seria activității chimice a metalelor.
- Aluminiul poate scoate orice metal aflat după el în serie (Zn, Fe, Pb, Cu, Hg, Ag) din compușii acestora
- Aluminiul nu poate scoate potasiul (K), calciul (Ca), sodiul (Na), magneziul (Mg) din compușii lor.
I. Reacția de ardere a metalelor:
👀 Experiment: Arderea sodiului
🔥 Atenție! Experiment demonstrativ efectuat numai de către profesor!
🔥 Atenție! Sodiul se aprinde violent în aer!
🔥 Atenție! Este obligatorie purtarea ochelarilor de protecție!
Materiale necesare:
Sodiu, cristalizor uscat, clește metalic,hârtie de filtru, pâlnie.
Descrierea experimentului:
- Cu multă grijă taie o bucățică mică de sodiu sub petrol ( metalele alcaline, fiind foarte reactive, se păstrează sub petrol).
- Cu un clește pune bucățica de sodiu în cristalizor, curăță-i stratul de oxid cu hârtia de filtru și acoperă cu pâlnia. Ce observi ?
Sodiul reacționează energic cu oxigenul din aer.
Concluzia experimentului:
Sodiul reacționează la rece și extrem de violent cu oxigenul, cu formare de oxid de sodiu – Na2O.
I. Reacția de ardere a metalelor:
👀 Experiment: Arderea magneziului cu o flacără orbitoare
🔥 Atenție! când lucrezi cu surse de încălzire!
🔥 Atenție! Nu privi flacăra orbitoare decât câteva secunde! Altfel, îți poate afecta vederea!
🔥 Atenție! Pilitura de magneziu este inflamabilă!
🔥 Atenție! Ai grijă să nu te arzi de la așchiile incandescente!
Materiale necesare:
Spirtieră, panglică (pilitură) de magneziu, chibrit, clește metalic
Descrierea experimentului:
- Încălzește panglica de magneziu, cu ajutorul unui clește, în flacăra spirtierei. Dacă ai pulbere de magneziu, presar-o direct în flacăra spirtierei.
- Ce observi ?
Panglica de magneziu se aprinde și arde cu o flacără extrem de strălucitoare. În urma arderii se obține o pulbere albă.
Concluzia experimentului:
Magneziul arde cu oxigenul din aer cu o flacără orbitoare, formând oxid de magneziu, de culoare albă. Aceasta este o reacție de combinare, întrucât avem un singur produs de reacție.
2Mg + O2 = 2MgO (Oxid de magneziu)
I. Reacția de ardere a metalelor:
👀 Experiment: Arderea aluminiului
🔥 Atenție! când lucrezi cu surse de încălzire!
🔥 Atenție! Pilitura de aluminiu este inflamabilă!
🔥 Atenție! Ai grijă să nu te arzi de la așchiile incandescente!
Materiale necesare:
Spirtieră, pilitură de aluminiu, chibrit, spatulă.
Descrierea experimentului:
- Presară pilitură de aluminiu în flacăra spirtierei
- Ce observi ?
Pilitura de aluminiu se aprinde în oxigen și arde cu scântei strălucitoare.
Concluzia experimentului:
Aluminiul se combină cu oxigenul din aer, la cald și formează oxidul de aluminiu
4Al + 3O2 = 2Al2O3 (Oxid de aluminiu)
II. Reacția metalelor cu apa
👀 Experiment: Reacția sodiului cu apa
🔥 Atenție! Experiment demonstrativ efectuat numai de către profesor!
🔥 Atenție! Sodiul se poate aprinde în aer!
🔥 Atenție! Se formează hidroxid de sodiu extrem de caustic!
🔥 Atenție! Se formează hidrogen care poate exploda în oxigenul din aer!
Materiale necesare:
Cristalizor, apă, sodiu, fenolftaleină, clește metalic, pâlnie, chibrit.
Descrierea experimentului:
- Pune în cristalizor puțină apă și adaugă câteva picături de fenolftaleină.
- Cu multă grijă taie o bucățică mică de sodiu sub petrol (metalele alcaline, fiind foarte reactive, se păstrează sub petrol).
- Cu un clește pune bucățica de sodiu în apa din cristalizor și acoperă cu pâlnia. Vino cu un băț de chibrit aprins deasupra pâlniei.
- Ce observi ?
Sodiul reacționează energic cu apa, înroșind fenolftaleina și când apropiem flacăra chibritului de pâlnie, are loc o pocnitură explozivă.
Concluzia experimentului:
Sodiul reacționează la rece și extrem de violent cu apa, cu formare de hidroxid de sodiu – NaOH (a înroșit fenolftaleina) și hidrogen –H2 (arde cu explozie în aer).
2Na + 2H2O = 2NaOH + H2 ↑
II. Reacția metalelor cu apa
👀 Experiment: Reacția magneziului cu apa
🔥 Atenție! când lucrezi cu surse de foc !
Materiale necesare:
Eprubetă, apă, pulbere de magneziu, fenolftaleină, clește de lemn, chibrit, spirtieră, spatulă.
Descrierea experimentului:
- Pune în eprubetă puțină apă și adaugă câteva picături de fenolftaleină.
- Cu spatula pune puțină pulbere de magneziu în apă.
- Cu un clește de lemn ține eprubeta în flacăra spirtierei, rotind-o continuu.
- Vino cu un băț de chibrit aprins deasupra eprubetei
- Ce observi ?
Magneziul reacționează la cald cu apa, înroșind fenolftaleina și gazul rezultat arde în aer.
Concluzia experimentului:
Magneziul reacționează la cald cu apa, cu formare de hidroxid de magneziu – Mg(OH)2 (a înroșit fenolftaleina) și hidrogen –H2 (arde cu flacără în aer).
Mg + 2H2O = Mg(OH)2 + H2 ↑
🔦 Observație
O substanță care are caracter amfoter, reacționează atât cu bazele, cât și cu acizii (de exemplu hidroxidul de aluminiu, hidroxidul de zinc etc.).
III. Reacția metalelor cu săruri.
👀 Experiment: Reacția cuprului cu azotatul de argint
🔥 Atenție! azotatul de argint este toxic și caustic (îți poate provoca arsuri)!
Materiale necesare:
2 pahare Berzelius, spatulă, sârmă de cupru spiralată, soluție de azotat de argint, soluție de sulfat de cupru, argint.
Descrierea experimentului:
- Pune într-un pahar Berzelius sârma de cupru spiralată și toarnă peste sârmă soluție de azotat de argint.
- Pune în alt pahar Berzelius un obiect de argint și toarnă peste el soluție de sulfat de cupru. Reacție lentă. Așteaptă mai mult timp până are loc reacția
- Ce observi ?
Pe sârma de cupru se depune un metal argintiu. Argintul nu reacționează cu sulfatul de cupru.
Concluzia experimentului:
Reacția cuprului cu azotatul de argint- AgNO3 decurge cu formare de azotat de cupru II – Cu(NO3)2 și argint – Ag. În seria activității chimice, cuprul este înaintea argintului și poate scoate argintul din compușii săi. Argintul nu reacționează cu sulfatul de cupru, fiindcă argintul este după cupru și nu îl poate scoate din compușii săi.
Cu + 2AgNO3 = Cu(NO3)2 + 2Ag ↓
Ag nu reacționează cu sărurile de cupru.