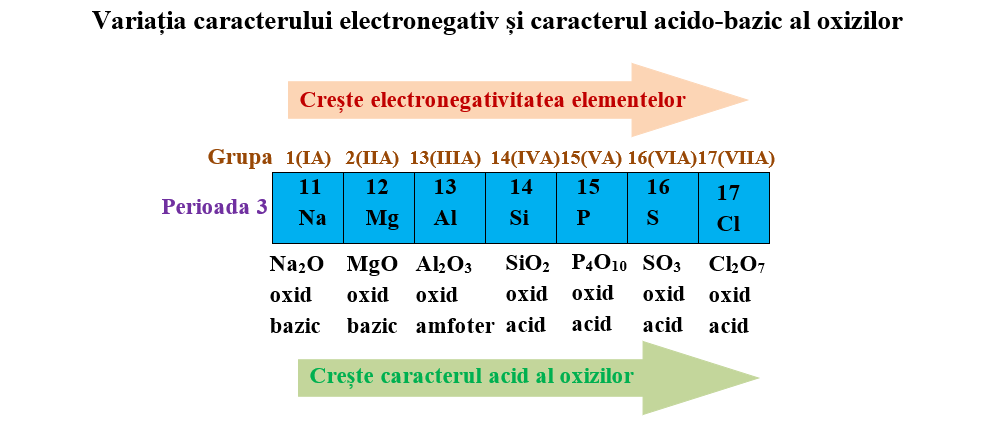
III.3. Caracterul nemetalic și electronegativ.
Nemetalele au caracter chimic nemetalic și caracter electrochimic electronegativ (formează ioni negativi prin acceptare de electroni).
Atomii nemetalelor având un număr mare de electroni pe ultimul strat, acceptă electroni pentru a forma octet stabil pe stratul de valență, identic cu cea a gazului rar ulterior lui în Sistemul periodic.
Prin acceptare de electroni atomii nemetalelor devin ioni negativi (anioni), deoarece vor avea un surplus de electroni în înveliș. Spunem că nemetalele au un caracter electronegativ.
Formarea ionilor negativi:
E + n ē → E-n (Ion negativ sau anion)
unde E = nemetal, n = nr. electroni acceptați = sarcina ionului
- Nemetalele din grupa a 15 a (a V A) au 5 ē de valență și trebuie să accepte 3 ē pentru a ajunge la configurația stabilă de octet, formând ioni negativi cu sarcina - 3.

- Nemetalele din grupa a 16 a (a VIA) au 6 ē de valență și trebuie să accepte 2 ē pentru a ajunge la configurația stabilă de octet, formând ioni negativi cu sarcina - 2.

- Nemetalele din grupa a 17 a (a VII A) au 7 ē de valență și trebuie să accepte 1 ē pentru a ajunge la configurația stabilă de octet, formând ioni negativi cu sarcina - 1.

🔦 Observație
Au caracter nemetalic elementele caracterizate prin energie de ionizare mare, care nu pot realiza configurații stabile prin cedare de electroni.
Caracterul nemetalic:
-
Crește cu creșterea sarcinii nucleare (Z), deoarece crește atracția nucleului asupra electronilor periferici.
-
Crește cu scăderea distanței dintre nucleu și electronii de valență, deoarece crește atracția nucleului asupra electronilor periferici.

🔦 Observație
Fluorul este cel mai electronegativ element chimic.
Nemetalele se găsesc în Sistemul periodic deasupra liniei îngroșate (linia zig-zag).
👀 Experimente
Cele mai importante proprietăți chimice ale clorului (nemetal cu un caracter electronegativ pronunțat):
1. Reacția clorului cu metalele:
x Cl2 + 2 Me → 2 MeClx
2. Reacția clorului cu hidrogenul:
Cl2 + H2 → 2 HCl (Acid clorhidric)
3. Reacția clorului cu apa:

4. Reacția clorului cu bazele tari:
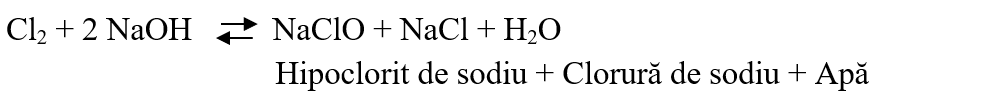
5. Reacția clorului cu sărurile halogenilor cu caracter electronegativ mai slab decât clorul (bromuri, ioduri).
1. Reacția clorului cu metalele: x Cl2 + 2 Me → 2 MeClx
👀 Experiment: Reacția magneziului cu clorul
🔥 Atenție! Experiment demonstrativ efectuat numai de către profesor!
🔥 Atenție! Experimentul se realizează sub nișă!
🔥 Atenție! Nu inspira clorul! Este extrem de toxic și îți poate afecta plămânii!
Materiale necesare:
Pahar Berzelius, clorat de potasiu, acid clorhidric concentrat, magneziu pulbere, lingură de ars, spirtieră, chibrit, sticlă de ceas, spatulă .
Descrierea experimentului:
- Pune în pahar un vârf de spatulă și adaugă câteva picături de acid clorhidric concentrat. Acoperă imediat paharul cu o sticlă de ceas
- Ce observi ?
Se degajă un gaz galben- verzui.
Cloratul de potasiu cu acidul clorhidric produce clor gazos.
KClO3 + 6HCl = KCl + 3H2O + 3Cl2 ↑
- Încălzește în lingura de ars pulberea de magneziu până la incandescență.
- Introdu magneziu incandescent în paharul cu clor.
- Ce observi ?
Magneziul reacționează cu clorul .
Concluzia experimentului:
Magneziul reacționează cu clorul, la cald și formează clorura de magneziu, sub forma unui gaz alb.
Mg + Cl2 = MgCl2 (Clorură de magneziu)
5. Reacția clorului cu sărurile halogenilor cu caracter electronegativ mai slab decât clorul (bromuri, ioduri).
👀 Experiment: Reacția clorului cu bromura și iodura de potasiu
🔥 Atenție! Experiment demonstrativ efectuat numai de către profesor!
🔥 Atenție! Experimentul se realizează sub nișă!
🔥 Atenție! Nu inspira clorul, bromul și iodul!
🔥 Atenție! Clorul, bromul și iodul sunt extrem de toxici și îți pot afecta grav plămânii !
🔥 Atenție! Acidul clorhidric este extrem de caustic!
Materiale necesare:
Pahare Berzelius și Erlenmeyer,dop perforat cu tub și furtun, clorat de potasiu, acid clorhidric concentrat, soluție de bromură de potasiu, soluție de iodură de potasiu, spatule .
Descrierea experimentului:
- Pune în pahar un vârf de spatulă și adaugă câteva picături de acid clorhidric concentrat.
- Acoperă imediat paharul cu o sticlă de ceas.
- Ce observi ?
Se degajă un gaz galben- verzui.
Cloratul de potasiu cu acidul clorhidric produce clor gazos.
KClO3 + 6HCl = KCl + 3H2O + 3Cl2 ↑
-
Acoperă paharul unde ai obținut clor cu dop și tub cu furtun și introdu-l în soluția de bromură de potasiu.
-
Ce observi?
La barbotarea clorului în bromura de potasiu se observă o colorație brună.
-
Acoperă paharul unde ai obținut clor cu dop și tub cu furtun și introdu-l în soluția de iodură de potasiu.
-
Ce observi?
La barbotarea clorului în iodura de potasiu se observă o colorație violetă.
Concluzia experimentului:
Clorul reacționează cu soluția de bromură de potasiu și formează clorura de potasiu (KCl) și brom (Br2).
Cl2 + 2KBr → 2KCl + Br2
Clorul reacționează cu soluția de iodură de potasiu și formează clorura de potasiu (KCl) și iod (I2).
Cl2 + 2KI → 2KCl + I2
Întrucât clorul scoate bromul și iodul din sărurile lor, spunem că are un caracter electronegativ mai accentuat decât bromul și iodul.
Electronegativitatea unui element reprezintă capacitatea unui atom al elementului de a atrage electronii înspre el.
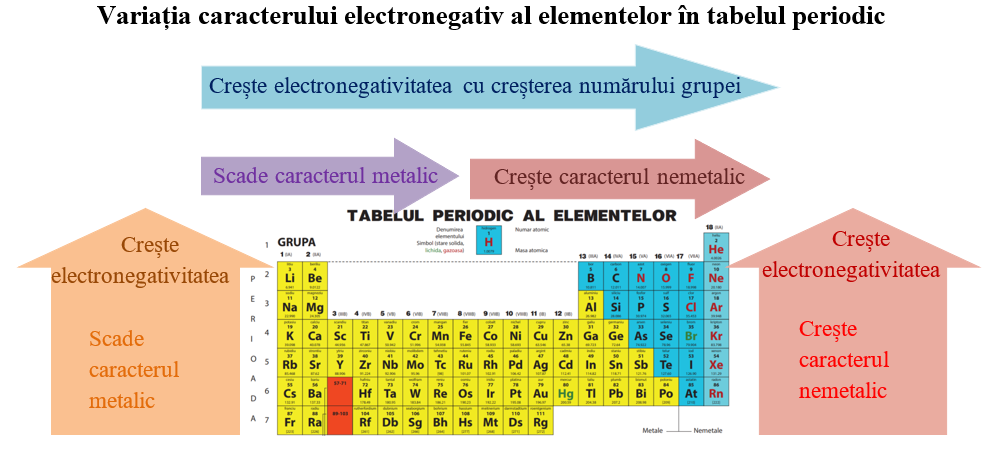
🔦 Observație
Trecerea de la un caracter metalic la caracterul nemetalic în Sistemul periodic se face gradat prin intermediul semimetalelor (siliciu, germaniu, arsen), care au atât proprietăți de metal, cât și proprietăți de nemetal.
Variația periodică a electronegativității în Tabelul periodic determină nu numai caracterul metalic și nemetalic al elementelor, ci și variația proprietăților compușilor elementelor chimice. De exemplu, variația caracterului acido-bazic al oxizilor elementelor chimice.