III.1.4. Etanolul.
Etanolul (denumit și alcool etilic sau mai simplu doar alcool) este un compus organic din clasa alcoolilor, fiind principalul alcool întâlnit în băuturile alcoolice. Are formula chimică C2H5OH, care poate fi scrisă desfășurat CH3–CH2–OH, fiind din punct de vedere structural alcătuit dintr-un radical etil, legat de o grupă hidroxil. Etanolul are formula structurală:
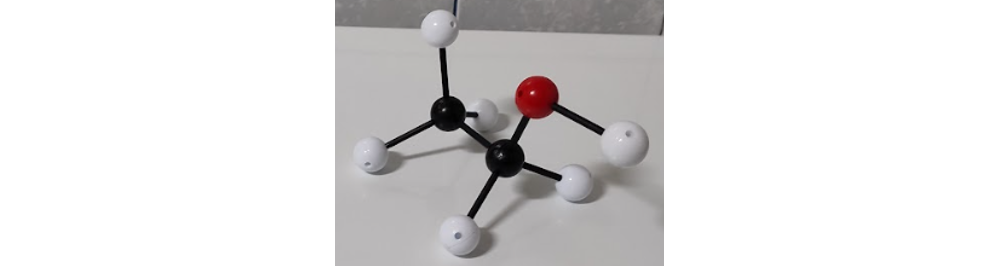
III.1.4.1. Obținerea etanolului.
Etanolul din compoziția băuturile alcoolice se obține exclusiv prin fermentația alcoolică. Unele specii de drojdii (precum Saccharomyces cerevisiae) metabolizează glucoza și polizaharidele obținându-se etanol și dioxid de carbon:
C6H12O6 → 2C2H5OH + 2CO2 ↑
C12H22O11 + H2O → 4C2H5OH + 4CO2 ↑
👀 Experiment: Obținerea etanolului și fermentația alcoolică
Materiale necesare:
Mere, borcan, răzătoare, tifon, hârtie indicator universal de pH.
Descrierea experimentului:
- Pune merele spălate și rase în borcan, adaugă apă cât să le acopere și o linguriță de zahăr.
- Acoperă borcanul cu tifon și lasă-l în aer liber. Lăsă merele să fermenteze. Temperatura din încăpere trebuie să fie de minim 22°C. Amestecă-le de 1-2 ori pe zi.
- Când apare mirosul caracteristic alcoolului s-a încheiat fermentația alcoolică.
Concluzia experimentului:
Fermentația alcoolică este procesul prin care se formează alcool etilic și dioxid de carbon, sub acțiunea diferitelor microorganisme (drojdiile genului Saccharomyces sp, Bacillus macerans), asupra diferitelor substanțe, mai ales glucide.
Ecuația chimică a fermentației alcoolice este:

Pentru a evidenția formarea alcoolului etilic vom realiza reacția de oxidare blândă a etanolului cu dicromat de potasiu și acid sulfuric.
Materiale necesare:
Alcool etilic, dicromat de potasiu, acid sulfuric concentrat, eprubetă, pahare Berzelius, spirtieră, clește de lemn, chibrit.
Descrierea experimentului:
- Dizolvă un vârf de spatulă (0,2 g) de dicromat de potasiu în 2-3 mL apă și apoi adaugă în această soluție 2-3 picături de acid sulfuric;
- Pune această soluție acidulată într-o eprubetă și adaugă câteva soluția de alcool etilic obținută prin fermentație. Încălzește ușor în flacăra unei spirtiere cu ajutorul cleștelui de lemn.
- Rotește continuu eprubeta în flacără și ține-o cu gura îndreptată spre o parte unde nu se află nicio persoană.
- Lasă câteva minute să se răcească eprubeta.
- Ce observi?
Ionul dicromat Cr2O7-2 portocaliu trece la ionul crom(III) Cr+3 de culoare verde.
Ecuația reacției chimice:
3CH3CH2OH + K2Cr2O7 + 4H2SO4 → 3CH3CHO + K2SO4 + Cr2(SO4)3 + 7H2O
Etanol + bicromat de potasiu + acid sulfuric → acetaldehidă + sulfat de potasiu + sulfat de crom III + apă
Putem evidenția formarea etanolului prin distilarea amestecului fermentat, încălzind amestecul la o temperatură de 78,3 °C (temperatura de fierbere a etanolului) și apoi răcind vaporii rezultați. Prin distilare se separă componentele lichide ale unui amestec omogen pe baza punctelor lor de fierbere diferite. Acest amestec conține etanol cu p.f.(punctul de fierbere) de 78,3 °C și apa are p.f. de 100 °C, la presiune atmosferică normală. În timpul distilării vaporizăm alcoolul etilic la temperatura constantă de 78,3 °C și apoi condensăm vaporii săi prin răcire. Oprim distilarea când temperatura începe să crească.
III.1.4.2. Proprietățile fizice ale etanolului.
Alcoolul etilic este:
- O substanță lichidă incoloră.
- Miscibil în apă în orice proporții. Solubilitatea se datorează grupării hidroxil din molecula alcoolului prin intermediul căreia între moleculele de apă și de alcool se stabilesc legături de hidrogen intermoleculare.
- Lichid volatil
- Miros caracteristic
- Gust arzător
- Cu densitatea mai mică decât a apei (789,4 kg/m3)
- Temperatura de fierbere mai mică decât a apei (78,37 °C).
III.1.4.3. Proprietățile chimice ale etanolului.
👀 Experiment: Reacția de ardere a alcoolului etilic
🔥 Atenție! Experiment efectuat numai de profesor!
🔥 Atenție! Alcoolul este inflamabil! Părul trebuie strâns la spate și nu purta haine cu mâneci largi!
Materiale necesare:
Alcool etilic (spirt), sticlă de ceas, chibrit.
Descrierea experimentului:
- Se pune 1-2 mL de alcool în sticla de ceas
- Se aprinde alcoolul cu bățul de chibrit.
- Ce observi ?
Alcoolul este inflamabil, arzând în aer(oxigen) cu o flacără albastră.
Concluzia experimentului:
Alcoolul (C2H5OH) în reacție cu oxigenul din aer formează apă și dioxid de carbon, care stinge
bățul de chibrit.
C2H5OH + 3O2 = 3H2O + 2CO2 ↑
👀 Experiment: Foc fără chibrit
🔥 Atenție! Acest experiment se efectuează numai de către profesor purtând echipament de protecție (ochelari de
protecție, mănuși de protecție)! Reacția este puternic exotermă !
🔥 Atenție! Acidul sulfuric este extrem de caustic, nociv și periculos pentru mediu acvatic !
🔥 Atenție! Permanganatul de potasiu este oxidant, nociv și periculos pentru mediu acvatic!
🔥 Atenție! Amestecul dintre acidul sulfuric și permanganatul de potasiu este extrem de inflamabil și după
experiment trebuie neutralizat cu soluție de hidroxid de sodiu!
Materiale necesare:
Acid sulfuric concentrat, permanganat de potasiu, alcool etilic, capsulă, spatulă, baghetă care are înfășurată vată
la un capăt.
Descrierea experimentului:
- În capsulă se introduce un vârf de spatulă de KMnO4 solid peste care se toarnă 2-3 picături de H2SO4 concentrat.
- Introducem bagheta, care are înfășurată vată la un capăt, în C2H5OH și apoi o apropiem de amestecul din capsulă.
- Ce observi?
Vata îmbibată cu alcool începe să ardă cu flacără, fără să folosim chibrit pentru aprindere.
Concluzia experimentului:
În urma reacției dintre permanganatul de potasiu și acidul sulfuric se obține heptaoxidul de dimangan, care este instabil și se descompune în dioxid de mangan și oxigen, după următoarele reacții :
2 KMnO4 + H2SO4 → H2O + K2SO4 + Mn2O7
2 Mn2O7 → 4 MnO2 + 3 O2 ↑
Oxigenul aprinde alcoolul etilic, care arde cu flacără după următoarea reacție :
C2H5OH + 3 O2 → 3 H2O + 2 CO2 ↑
👀 Experiment: Licurici chimici
🔥 Atenție! Acest experiment se efectuează numai de către profesor purtând echipament de protecție (ochelari de
protecție, mănuși de protecție)! Reacția este puternic exotermă !
🔥 Atenție! Acidul sulfuric este extrem de caustic, nociv și periculos pentru mediu acvatic !
🔥 Atenție! Permanganatul de potasiu este oxidant, nociv și periculos pentru mediu acvatic!
🔥 Atenție! Amestecul dintre acidul sulfuric și permanganatul de potasiu este extrem de inflamabil și după
experiment trebuie neutralizat cu soluție de hidroxid de sodiu!
Materiale necesare:
Acid sulfuric concentrat, permanganat de potasiu, alcool etilic, eprubetă, clește de lemn, spatulă.
Descrierea experimentului:
- În eprubetă toarnă câțiva mililitri de H2SO4 concentrat.
- Peste acid prelinge cu grijă pe pereții eprubetei câțiva mililitri de C2H5OH. Întrucât alcoolul are densitatea mai mică decât acidul, el va forma un strat distinct deasupra celui de acid.
- Pune un vârf de spatulă de KMnO4 solid în pahar peste cele două lichide. Cristalele de permanganat de potasiu se vor așeza între cele două straturi de lichide.
- Așteaptă câteva minute și observă (cu ochelari de protecție) ce se întâmplă sub stratul de alcool.
- Ce observi?
Alcoolul începe să ardă cu scântei la suprafața de separare dintre acid și alcool.
Concluzia experimentului:
În urma reacției dintre permanganatul de potasiu și acidul sulfuric se obține heptaoxidul de dimangan, care este instabil și se descompune în dioxid de mangan și oxigen, după următoarele reacții :
2 KMnO4 + H2SO4 → H2O + K2SO4 + Mn2O7
2 Mn2O7 → 4 MnO2 + 3 O2 ↑
Oxigenul aprinde alcoolul etilic, care arde cu scântei după următoarea reacție :
C2H5OH + 3 O2 → 3 H2O + 2 CO2 ↑
👀 Experiment: Reacția de oxidare a etanolului în acetaldehidă
🔥 Atenție! Experiment efectuat numai de profesor!
��🔥 Atenție! Alcoolul este inflamabil! Părul trebuie strâns la spate și nu purta haine cu mâneci largi!
🔥 Atenție! Iodul este o substanță corozivă: contactul iodului cu pielea și membranele mucoase cauzează arsuri severe!
🔥 Atenție! Vaporii de iod cauzează iritații pulmonare severe, care pot conduce la edem pulmonar!
🔥 Atenție! Soda (NaOH) este caustică!
Materiale necesare:
Alcool etilic (spirt), soluție iod-iodură de potasiu, soluție de hidroxid de sodiu, chibrit, eprubetă, spirtieră, clește de lemn.
Descrierea experimentului:
- Se pune într-o eprubetă 1 mL de alcool etilic, cu 3 mL apă și se încălzește ușor la flacăra spirtierei.
- Se adaugă în această soluție 1 mL soluție de iod-iodură de potasiu și se toarnă soluție de sodă caustică până dispare colorația.
I2 + 2NaOH = NaI + NaOI + H2O
Concluzia experimentului:
Hipoioditul de sodiu(NaOI) este un oxidant puternic și transformă alcoolul etilic în aldehidă acetică.
C2H5OH + NaOI = CH3-CHO + NaI + H2O
👀 Experiment: Reacția de oxidare blândă a alcoolului (etanolului) cu dicromat de potasiu și acid sulfuric.
🔥 Atenție! Experiment efectuat numai de profesor! Părul trebuie strâns la spate și nu purta haine cu mâneci largi!
🔥 Atenție! Dicromatul de potasiu (K2Cr2O7) este coroziv, oxidant, foarte toxic, nociv, periculos pentru mediu.
🔥 Atenție! Acidul sulfuric, H2SO4, este caustic.
🔥 Atenție! Alcoolul etilic, CH3CH2OH, este inflamabil.
🔥 Atenție! Sulfatul de crom III, Cr2(SO4)3, este caustic și periculos pentru mediu.
🔥 Atenție! Acetaldehida, CH3CHO, este caustică și inflamabilă.
Materiale necesare:
Alcool etilic 96%, dicromat de potasiu, acid sulfuric concentrat, eprubetă, pahare Berzelius, spirtieră, clește de lemn, chibrit.
Descrierea experimentului:
- Dizolvă un vârf de spatulă (0,2 g) de dicromat de potasiu în 2-3 mL apă și apoi adaugă în această soluție 2-3 picături de acid sulfuric;
- Pune această soluție acidulată într-o eprubetă și adaugă câteva picături de alcool etilic 96%. Încălzește ușor în flacăra unei spirtiere cu ajutorul cleștelui de lemn.
- Rotește continuu eprubeta în flacără și ține-o cu gura îndreptată spre o parte unde nu se află nicio persoană.
- Lasă câteva minute să se răcească eprubeta.
- Ce observi?
Ionul dicromat Cr2O7-2 portocaliu trece la ionul crom(III) Cr+3 de culoare verde.
Ecuația reacției chimice:
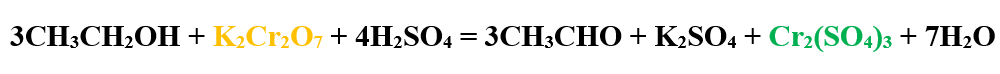
Concluzia experimentului:
La oxidarea blândă cu dicromat de potasiu în soluție acidulată cu acid sulfuric, alcoolii primari se transformă în aldehide.
Combinația dintre alcool și conducerea autovehiculelor este una foarte periculoasă. Din acest motiv, ȋn majoritatea țărilor, concentrația alcoolului ȋn sânge nu este permisă.
Polițiștii au ȋn dotare aparate pentru testarea alcoolemiei, numite ”etiloteste”. Etilotestul este de fapt un tub mic, închis la ambele capete cu dopuri, ce conține dicromat de potasiu în mediu de acid sulfuric condiționat pe silicagel. În prezența alcoolului pe care un șofer îl expiră prin tub are loc o reacție care transformă culoarea portocalie ȋn verde. Vaporii de alcool sunt conduși peste silicagelul îmbibat cu dicromat de potasiu în mediu acid. Acesta oxidează alcoolul la aldehidă, agentul oxidant trecând de la dicromat Cr2O7-2 portocaliu la crom(III) Cr+3 de culoare verde.
👀 Experiment: Reacția de oxidare blândă a alcoolului cu dicromat de potasiu și acid clorhidric
🔥 Atenție! Acidul clorhidric este caustic și periculos pentru mediu acvatic!
🔥 Atenție! Acetaldehida este inflamabilă și nocivă!
🔥 Atenție! Clorura de crom poate fi corosivă pentru metale, este nocivă în caz de înghițire, poate provoca o reacţie alergică a pielii și este toxică pentru mediul acvatic cu efecte pe termen lung!
🔥 Atenție! Alcoolul etilic, CH3CH2OH, este inflamabil.
Materiale necesare:
Alcool etilic, dicromat de potasiu, acid clorhidric concentrat, capsulă, spatulă.
Descrierea experimentului:
- Pune într-o capsulă un vârf de spatulă de dicromat de potasiu și apoi adaugă, picătură cu picătură acidul clorhidric concentrat până umectezi bine toate cristalele de dicromat.
- Adaugă cu pipeta etanolul, picătură cu picătură, agitând amestecul după ce pui câteva picături.
- Etanolul se adaugă până la apariția unei soluții verzi.
- Ce observi?
Soluția obținută emană vapori cu miros de mere verzi.
Concluzia experimentului:
La oxidarea blândă cu dicromat de potasiu în soluție acidulată cu acid clorhidric, alcoolii primari se transformă în aldehide.
Ionul dicromat Cr2O7-2 (portocaliu) în mediu acid (acid clorhidric concentrat) trece la ionul crom III Cr+3 de culoare verde și se degajă acetaldehidă, cu miros de mere verzi.
3 C2H5OH + K2Cr2O7 + 8 HCl → 3 CH3CHO + 2 CrCl3 + 2 KCl + 7 H2O
Reacția are loc chiar la temperatura camerei.
👀 Experiment: Reac�ția alcoolului etilic cu permanganatul de potasiu
🔥 Atenție! Experiment efectuat numai de profesor!
🔥 Atenție! Alcoolul este inflamabil! Părul trebuie strâns la spate și nu purta haine cu mâneci largi!
🔥 Atenție! Permanganatul de potasiu este oxidant, nociv și periculos pentru mediu!
🔥 Atenție! Acidul sulfuric este caustic!
Materiale necesare:
Alcool etilic (spirt), soluție de acid sulfuric diluat, permanganat de potasiu, chibrit, eprubetă, dop cu tub, spirtieră, clește de lemn.
Descrierea experimentului:
- Se pune într-o eprubetă câteva cristale de permanganat de potasiu, 1-2 mL apă și 2 mL de alcool etilic.
- Se fierbe 2 min acest amestec și se adaugă 3 mL acid sulfuric diluat. Se atașează eprubetei dopul cu tub și se continuă încălzirea.
🔥 Atenție! Reacția este efervescentă și poate arunca din conținutul eprubetei în afara ei!
- Ce observi ?
Alcoolul etilic se poate oxida cu formare de acid acetic cu mirosul caracteristic(oțet).
Concluzia experimentului:
Reacția alcoolului etilic cu permanganatul de potasiu în mediu acid duce la formarea intermediară a acetaldehidei și mai apoi la formarea acidului acetic (CH3COOH).
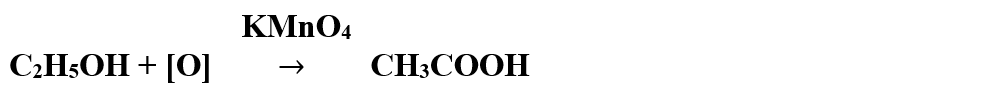
Alcoolul este metabolizat de ficat, care are sarcina de a scăpa de substanțele toxice. Un consum ridicat de alcool poate suprasolicita ficatul producând boli ale acestuia (ciroză hepatică), boli cardiovasculare, boli digestive, cancere, distruge celulele creierului.
Reacția de oxidare a etanolului în corpul uman are loc cu ajutorul unei enzime din ficat numită alcool-dehidrogenază (ADH) formând acetaldehidă. Oxidarea acetaldehidei în acid acetic este catalizată de o altă enzimă numită aldehid-dehidrogenază-2 (ALDH2). Corpul poate excreta acidul acetic sau sarea sa, acetatul, sau îl poate transforma în energie (de aceea alcoolul are multe calorii).
Știați că:
-
Un număr mare de asiatici nu pot secreta enzima numită aldehid-dehidrogenază-2 (ALDH2) și prin urmare eliminarea acetaldehidei este foarte lentă. Urmările sunt destul de neplăcute : culoarea roșie a pielii, greață, palpitații ale inimii și amețeală.
-
Există foarte puțini oameni care suferă de sindromul autofermentației alcoolice. Aceștia au în intestin o ciupercă numită drojdie de bere (Saccharomyces cerevisiae) care transformă carbohidrații (dulciuri, pâine etc.) ingerați în alcool.
👀 Experiment: Reacția de deshidratare a alcoolului etilic
🔥 Atenție! Experiment efectuat numai de profesor!
🔥 Atenție! Alcoolul este inflamabil! Părul trebuie strâns la spate și nu purta haine cu mâneci largi!
🔥 Atenție! Acidul sulfuric este caustic!
🔥 Atenție! Eterul rezultat în urma reacției este extrem de volatil și inflamabil!
Materiale necesare:
Alcool etilic (spirt), soluție de acid sulfuric concentrat, chibrit, eprubetă, dop cu tub, spirtieră, clește de lemn.
Descrierea experimentului:
- Se pune într-o eprubetă 2 mL alcool etilic și 2 mL de acid sulfuric concentrat, picătură cu picătură. Se încălzește puțin, cu atenție, amestecul.
- Se adaugă în eprubetă încă 2 mL de alcool etilic. Se astupă eprubeta cu dop prevăzut cu tub și se continuă încălzirea. Se aduce la gura tubului un chibrit aprins.
- Ce observi ?
Alcoolului etilic cu acid sulfuric formează eterul care este volatil și se aprinde ușor (inflamabil).
Concluzia experimentului:
Reacția de deshidratare a alcoolului etilic cu formarea eterului în prezența substanțelor avide de apă (acid sulfuric).
2C2H5OH → C2H5-O-C2H5 + H2O
👀 Experiment: Reacția alcoolului etilic cu acid clorhidric
🔥 Atenție! Experiment efectuat numai de profesor!
🔥 Atenție! Alcoolul este inflamabil! Părul trebuie strâns la spate și nu purta haine cu mâneci largi!
🔥 Atenție! Acidul sulfuric este caustic!
🔥 Atenție! Clorura de etil rezultată în urma reacției este extrem de volatilă și inflamabilă!
Materiale necesare:
Alcool etilic (spirt), soluție de acid sulfuric concentrat, clorură de sodiu, chibrit, eprubetă, dop cu tub, spirtieră, clește de lemn.
Descrierea experimentului:
- Se pune într-o eprubetă câteva cristale de clorură de sodiu, 2 mL alcool etilic și 2 mL acid sulfuric concentrat.
- Atașăm eprubetei un dop cu tub.
- Încălzim cu atenție eprubeta până când lichidul începe să fiarbă.
- Apropiem de capătul tubului un chibrit aprins.
- Ce observi ?
Clorura de etil formată arde cu o flacără verde.
Concluzia experimentului:
Reacția alcoolului etilic cu acid clorhidric are loc cu formarea clorurii de etil (C2H5 – Cl)
2NaCl + H2SO4 = Na2SO4 + 2HCl
C2H5OH + HCl = C2H5-Cl + H2O
👀 Experiment: Reacția de esterificare a alcoolului etilic cu acid acetic
🔥 Atenție! Experiment efectuat numai de profesor!
🔥 Atenție! Alcoolul este inflamabil! Părul trebuie strâns la spate și nu purta haine cu mâneci largi!
🔥 Atenție! Acidul acetic glacial este coroziv, vaporii săi provocând iritarea conjunctivei oculare și a căilor respiratorii, putând merge până la congestia pulmonară. Este inflamabil la o temperatură mai mare de 39 °C, caz în care poate forma un amestec explozibil cu aerul peste această temperatură.
🔥 Atenție! Acidul sulfuric este caustic!
🔥 Atenție! Acetatul de etil rezultat în urma reacției este volatil și inflamabil!
Materiale necesare:
Alcool etilic, acid acetic glacial, acid sulfuric concentrat, chibrit, eprubetă, dop perforat prevăzut cu tub de sticlă, spirtieră, clește de lemn.
Descrierea experimentului:
- Se pune într-o eprubetă 2 mL alcool etilic, 2 mL de acid sulfuric concentrat și 2 mL acid acetic.
- Încălzim cu atenție eprubeta până când lichidul începe să fiarbă. Cu un chibrit aprins venim la gura tubului
- Ce observi ?
Acetatul de etil format are un miros specific dulce fructat.
Concluzia experimentului:
Reacția alcoolului etilic cu acid acetic are loc cu formarea acetatului de etil (CH3COOC2H5) și apă.
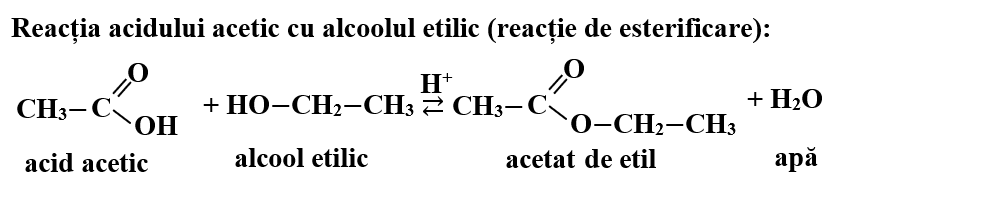
Reacția de esterificare este catalizată de acizi tari (HCl sau H2SO4).
Reacțiile de esterificare sunt reacții reversibile. Acetatul de etil poate reacționa cu apa rezultată cu refacerea reactanților inițiali (reacție de hidroliză).
Acetatul de etil este un lichid incolor, cu miros dulce de fructe și e folosit în lipiciuri, la decafeinizarea ceaiului și cafelei, odorant pentru esențe artificiale cu aromă de fructe, ca solvent pentru lacuri și nitroceluloză, curățarea ojei etc.
👀 Experiment: Reacția de esterificare dintre acid benzoic și etanol
🔥 Atenție! Experiment efectuat numai de profesor!
🔥 Atenție! Acidul benzoic este caustic, nociv și iritant!
🔥 Atenție! Alcoolul etilic este un lichid inflamabil!
🔥 Atenție! Acidul sulfuric este extrem de caustic, oxidant (poate agrava un incendiu), toxic și periculos pentru mediu!
🔥 Atenție! Benzoatul de etil este extrem de inflamabil!
Materiale necesare:
Eprubetă cu dop perforat și tub, acid benzoic, etanol, acid sulfuric, pipetă, spirtieră, clește de lemn.
Descrierea experimentului:
- Pune în eprubetă un vârf de spatulă de cristale de acid benzoic. Adaugă 10-15 ml de alcool etilic și 5-6 picături de acid sulfuric concentrat.
- Încălzește amestecul până vei observa dispari�ția cristalelor și mai continuă încă puțin până simți un miros fructat.
- Cu un chibrit încearcă aprinderea benzoatului de etil
- Ce observi ?
Benzoatul de etil este ușor volatil și inflamabil!
Concluzia experimentului:
Reacția dintre acidul benzoic și alcoolul etilic este o reacție de esterificare, care este un proces reversibil. Echilibrul poate fi deplasat spre dreapta prin luarea în exces a unuia dintre reactanți (etanolului) sau prin izolarea apei din amestecul reactant.
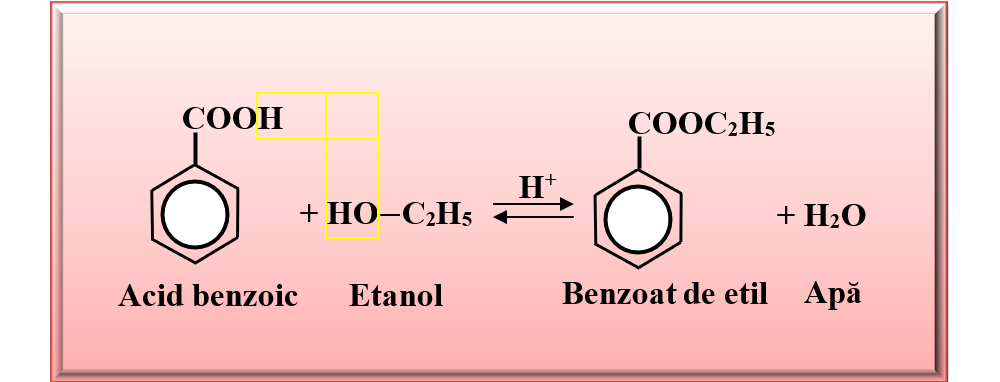
Benzoatul de etil este un ester organic, un lichid incolor, cu miros dulceag, floral-fructat (de zmeură-căpșuni). Este insolubil în apă și solubil în alcool, eter, cloroform etc. Are punctul de fierbere ≅ 212 °C.
Benzoatul de etil (E214) are diverse utilizări în :
-
industria alimentară, ca agent de aromă în băuturi alcoolice, sucuri de fructe, esențe artificiale;
-
cosmetică, drept conservant și ingredient în diverse parfumuri și esențe.
-
sinteză organică, ca solvent în reacții chimice.
👀 Experiment: Flacăra verde (Reacția etanolului cu acidul boric)
🔥 Atenție! Experiment efectuat numai de profesor!
🔥 Atenție! Alcoolul etilic este inflamabil!
🔥 Atenție! Acidul boric este iritant! Se va evita orice contact cu pielea, ochii şi inhalarea de vapori.
Materiale necesare:
Acid boric, alcool etilic, sticlă de ceas, chibrit, spatulă.
Descrierea experimentului:
- Pe o sticlă de ceas pune 2-3 g de acid boric.
- Adaugă peste acidul boric câțiva mL de etanol și amestecă cu o spatulă.
- Aprinde cu un chibrit amestecul.
- Ce observi ?
Amestecul arde cu o flacără verde.
Concluzia experimentului:
Acidul boric cu etanolul formează un ester, numit trietil borat, care arde cu o flacără verde.
H3BO3 + 3 C2H5OH ⇌ (C2H5O)3B + 3 H2O
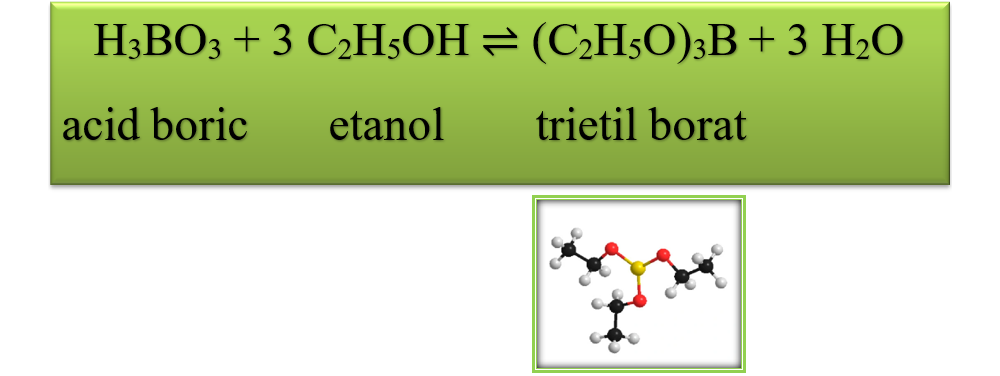
Acidul boric este unul dintre cei mai cunoscuți compuși ai borului, fiind folosit ca antiseptic, insecticid, ignifug pentru țesături etc.
Borul este un element chimic aflat în grupa a III a A, cu Z = 5. Are o răspândire mică în scoarța terestră (0,014%) sub formă de:



Acidul boric (H3BO3) se formează în scoarță prin descompunerea silicaților cu apă caldă etc.
Borul este un nemetal, având proprietăți asemănătoare cu carbonul și siliciul, cu o conductibilitate electrică mică la temperatura camerei, dar care crește odată cu temperatura.




Nitrura de bor și carbura de bor sunt compuși cu o duritate comparabilă ce cea a diamantului, folosiți în industria auto, aerospațială și fabricarea de scule.
Carbura de bor este folosită și la absorbția neutronilor în centralele nucleare, la armurile de corp și la blindajele de tancuri.
Încălzit la 700 °C, borul arde cu o flacără caracteristică de culoare roșie.
4 B + 3 O2 → 2 B2O3
Borul este un oligoelement care susține sănătatea celulară, funcțiile creierului, imunității, metabolizarea calciului, magneziului și fosforului în procesul de formare a oaselor, mărește nivelul estrogenului, împiedică formarea trombelor sangvine, creşte nivelul testosteronului etc.
Borul se găsește în prune, mere roșii, pere, piersici, struguri roșii, portocale, arahide, alune, avocado, fasole, năut, broccoli, cartofi, ceapă, morcovi, cafea, lapte etc.
Utilizările alcoolului etilic:
- Este folosit pe scară largă ca solvent (soluțiile de alcool fiind numite tincturi)
- Combustibil (la spirtiere, în laborator)
- Dezinfectant (alcool sanitar/spirt medicinal)
- Component de bază al băuturilor alcoolice
- Industria parfumurilor
- La termometre de cameră (colorat în roșu sau albastru)
- Sinteza unor medicamente
- Materie primă în sinteza unor compuși chimici.
Etanolul are următoarele efecte asupra organismului uman:
- Este un drog psihotrop care dă dependență, cauzând o intoxicație acută caracteristică, cunoscută sub numele de beție, când este consumat în cantități mari.
- Acţiune depresivă, sedativă şi tranchilizantă, deoarece încetinește funcționalitatea sistemului nervos central, blocând o parte din mesajele care ar trebui să ajungă la creier.
- Consumat excesiv, distruge celulele cerebrale pentru că determină reducerea cantității de apă necesare din ele. Astfel, apare o afectare a limbajului, a memoriei, alterează capacitatea de concentrare, abilitatea de exprimare coerentă, menținerea echilibrului.
- Acţiune diuretică și deshidratarea organismului, prin stimularea unor hormoni diuretici.
- Acțiune vasodilatatoare cu modificarea pulsului, tulburări ale termoreglării temperaturii corpului, palpitații, respirație dificilă etc.
- Duce la exces de acetaldehidă, compus toxic pentru organism. Cel mai expus este ficatul, locul unde se metabolizează peste 90% din alcoolul consumat și de aceea consumul zilnic suprasolicită sistemele enzimatice și atrage acumularea de produși toxici.